
| A、将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色 |
| B、SO2通入Fe2(SO4)3溶液中,无明显现象 |
| C、SO2通入已酸化的Ba(NO3)2溶液中,出现白色沉淀 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去 |


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
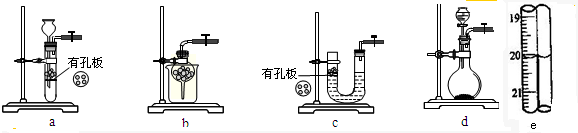
| 编号 | 1 | 2 | 3 |
| 消耗KI3溶液的体积/mL | 19.98 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
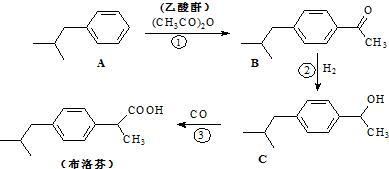
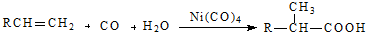
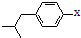 结构的酯类中共有6种(即X有不同的结构),请写出其中的二种
结构的酯类中共有6种(即X有不同的结构),请写出其中的二种查看答案和解析>>
科目:高中化学 来源: 题型:


 中官能团的名称
中官能团的名称 多一个碳的同系物,则满足下列条件的D的同分异构体共有
多一个碳的同系物,则满足下列条件的D的同分异构体共有| 浓硫酸 |
| 170℃ |
| Br2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于40. 00 mL |
| B、等于40.00 mL |
| C、大于10.00 mL |
| D、等于10.00 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向逆反应方向移动,N2和O2的转化率都减小 |
| B、平衡向正反应方向移动,N2和O2的转化率都增大 |
| C、压强增大平衡不移动,N2的转化率不变 |
| D、平衡向正反应方向移动,N2的转化率减小,O2的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com