
| A.pH=10的氨水稀释100倍 |
| B.pH=4的醋酸和pH=10的NaOH等体积混合 |
| C.pH=8的NaOH溶液与pH=8的Ba(OH)2等体积混合 |
| D.pH=11的NaOH溶液与pH=5的盐酸等体积混合 |
科目:高中化学 来源:不详 题型:实验题
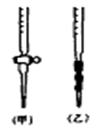
| A.用酸式滴定管取稀H2SO425.00mL,注入锥形瓶中,加入指示剂。 |
| B.用待测定的溶液润洗酸式滴定管 |
| C.用蒸馏水洗干净滴定管 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2—3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
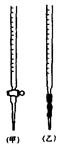
| A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤 |
| B.滴定前尖嘴部分有一气泡,滴定终点时消失 |
| C.定容时,俯视刻度线 |
| D.滴定前仰视读数,滴定后俯视读数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使用分光光度计,可以换算得到某溶液的浓度 |
| B.pH试纸是将试纸用多种酸碱指示剂的混合液浸透,经晾干后制成的 |
| C.在滴定过程中,滴加溶液的速度不能太快,一般以每秒3-4滴为宜 |
| D.移液管管尖残留的液体一定要用洗耳球吹出以保证移取液体体积的准确性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.其溶液中由水电离出的c(H+)的大小关系是① = ②>③>④>⑤ |
| B.其溶液中由水电离出的(H+)的大小关系是④>③>①= ⑤>② |
| C.上述溶液中能能促进水的电离是②>①=>⑤>③ |
| D.上述溶液中能促进水的电离是只有④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2CO(g)+O2 (g)=2CO2(g)△H = ―556kJ·mol-1 |
| B.CH4(g)+2O2(g)=CO2 (g)+2H2O (l)△H = ―890kJ·mol-1 |
| C.2H2 (g)+O2(g)=2H2O(l)△H = ―571.6kJ·mol-1[ |
| D.H2 (g)+Cl2(g)=2HCl(g)△H = ―184.6kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.13 | B.14 | C.15 | D.12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.13 | B.14 | C.15 | D.不能确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com