
(共8分)
Ⅰ.(2分)已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得溶液呈酸性;0.01 mol?L-1的HIO3或HMnO4溶液与pH=12的Ba(OH)2溶液等体积混合所得溶液均呈中性。
(1)H5IO6是 (填“强电解质”或“弱电解质”)。
(2)(6分)已知H5IO6和MnSO4在溶液中反应生成高锰酸、碘酸和硫酸,此反应中氧化剂是 (填化学式)。
Ⅱ.如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。
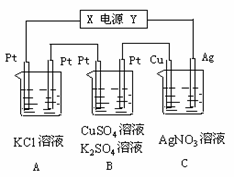 试回答:
试回答:
⑴ 电源电极X名称为____________。
⑵ pH变化:A池________________,
B池________________,
C池________________。
⑶ 写出B池中所发生的电解反应方程式:
_____________________________________________________________________。
科目:高中化学 来源:2012届上海市崇明县高三高考模拟考试(二模)化学试卷(带解析) 题型:填空题
(共8分) 有机物A为绿色荧光蛋白在一定条件下水解的最终产物之一,结构简式为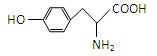
请回答下列问题:
(1)、关于A的性质推断错误的是 ;
a.A既能和酸反应又能和碱反应 b.A不能发生加成反应
c.A可以发生氧化反应 d.A不能通过缩聚反应得到高分子化合物
(2)、A与氢氧化钠溶液反应的化学方程式为 ;
(3)、符合下列4个条件A的同分异构体有 种;
① 1,3,5-三取代苯; ② 遇氢氧化铁溶液显紫色;
③ 氨基与苯环直接相连; ④ 属于酯类
(4)、写出符合上述题意的任意一种A的同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年内蒙古巴市一中高一上学期10月月考化学试卷 题型:填空题
(共8分,每空1分)看下列仪器装置图,回答下列问题: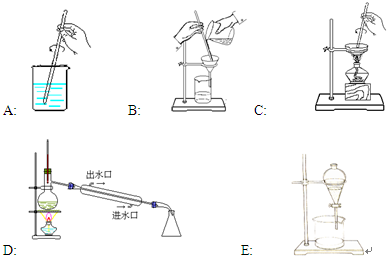
(1)写出上述各装置的名称:
| A.; | B.; | C.; |
| D.;E. |
查看答案和解析>>
科目:高中化学 来源:2014届甘肃永昌一中高二上学期期中考试文科化学试卷(解析版) 题型:填空题
(共8分)现有A、B、C、D、E、F六种物质,它们的相互转化关系如下图所示。已知A和B是单质,B、E、F在常温下为气体,C为淡黄色固体。

(1)写出A、B的化学式:A ,B
(2)写出A生成C的化学方程式
(3)写出C与D反应生成E的化学方程式
查看答案和解析>>
科目:高中化学 来源:2014届云南省昆明市高二9月月考化学试卷(解析版) 题型:填空题
(共8分)
在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)如图中表示NO2的变化的曲线是 。
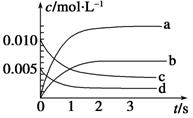
(2)求 2 s末用氧气表示的平均反应速率v(O2)=
(3)求达平衡时NO的转化率为
(4)能说明该反应已经达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正 d.容器内的密度保持不变
(5)能够使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出NO2气体 b.增大O2的浓度
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市普陀区高三上学期期末质量抽测化学试卷 题型:填空题
(本题共8分)
β型硼氮化合物—-(BN)n是一种无机合成材料[最简式为(BN)],具有高硬度、耐高温的特点,是做超高温耐热陶瓷材料、磨料、精磨刃具的好材料。用硼砂(Na2B4O7)与尿素在高温高压下反应可以获得。例如: Na2B4O7 + 2CO(NH2)2 → 4(BN) + Na2O + 2CO2
(1)、请用氧化物的形式表示硼砂的化学式 。β型(BN)n比晶体硅具有更高硬度和耐热性的原因是: 。
(2)、(1)上述反应式中具有4种不同能量电子的原子,它代表的元素在周期表中处于 周
期,第 族。
(2)能用于比较N与O非金属性相对强弱的事实是 。
A.最高价氧化物对应水化物的酸性 B.H2O(g) 比NH3(g)稳定
C.单质与H2反应的难易程度 D.NO中氮元素显正价,氧元素显负价
(3)、写出指定分子的电子式:生成物中含极性键的非极性分子 。
(4)、与硼同主族且相邻周期的元素,其单质与NaOH(aq)反应的离子方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com