
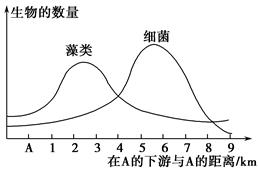
科目:高中化学 来源:不详 题型:填空题
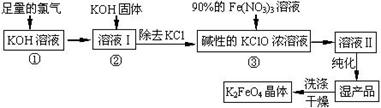
| A.与 “溶液I” 中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供反应物 |
| D.使副产物KClO3转化为 KClO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO2通入氢氧化钠溶液中制Na2CO3 |
| B.H2和Cl2光照制HCl |
| C.Cl2通入澄清石灰水中制漂白粉 |
| D.用硫黄制硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
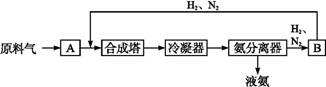
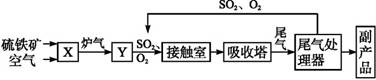
 2NH3(g) ΔH<0; 2SO2(g)+O2(g)
2NH3(g) ΔH<0; 2SO2(g)+O2(g) 2SO3(g) ΔH<0
2SO3(g) ΔH<0查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.漂白粉:2Cl2—Ca(ClO)2 | B.H2SO4:FeS2—2H2SO4 |
| C.氨:C—H2—2/3 NH3 | D.HNO3: NH3—HNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯碱工业中若阳极产生0.1mol氯气则通过溶液的电子的物质的量为0.2mol |
| B.1L 1mol/LNa2CO3溶液中阴离子和阳离子的总数为3×6.02×1023 |
C.当碳酸溶液的PH增大1时,溶液中 可能增大也可能减小 可能增大也可能减小 |
| D.乙烯和苯分子中都存在碳碳双键,都能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.土壤胶体吸附的H+、Al3+被其他阳离子交换 |
| B.微生物、细菌在利用土壤中的有机物时,会产生二氧化碳和多种有机酸 |
| C.微生物、细菌在利用土壤中物质时,将土壤中的NH3转化为亚硝酸和硝酸,将硫化物转化为硫酸 |
| D.土壤有机物中的氮被微生物分解生成氨的氨化过程,会使土壤的pH升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com