
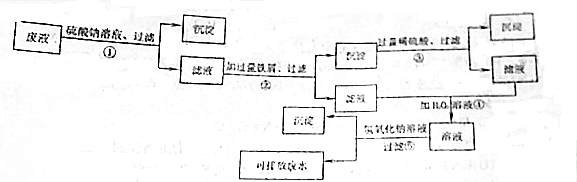
分析 含有Fe3+,Ba2+,Cu2+三种离子的废液中滴加硫酸钠溶液,因发生Ba2++SO42-=BaSO4↓,过滤除去硫酸钡沉淀,滤液里加入过量铁粉,将溶液里的Fe3+完全转化为Fe2+,同时可将Cu2+完全还原成Cu,发生的离子反应为2Fe3++Fe=3Fe2+和Fe+Cu2+=Fe2++Cu,过滤得到的不溶物为铜和过量的铁,步骤③用过量的酸溶解铁,过滤得到的沉淀为Cu,发生的离子反应为Fe+2H+=Fe2++H2↑,步骤④是在含有Fe2+的溶液里滴加过量的H2O2溶液,氧化得到Fe3+,发生的离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O,步骤⑤是在含有Fe3+的溶液里滴加氢氧化钠溶液得到Fe(OH)3红褐色沉淀,发生的离子反应为Fe3++3OH-=Fe(OH)3↓,据此分析解答.
解答 解:含有Fe3+,Ba2+,Cu2+三种离子的废液中滴加硫酸钠溶液,因发生Ba2++SO42-=BaSO4↓,过滤除去硫酸钡沉淀,滤液里加入过量铁粉,将溶液里的Fe3+完全转化为Fe2+,同时可将Cu2+完全还原成Cu,发生的离子反应为2Fe3++Fe=3Fe2+和Fe+Cu2+=Fe2++Cu,过滤得到的不溶物为铜和过量的铁,步骤③用过量的酸溶解铁,过滤得到的沉淀为Cu,发生的离子反应为Fe+2H+=Fe2++H2↑,步骤④是在含有Fe2+的溶液里滴加过量的H2O2溶液,氧化得到Fe3+,发生的离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O,步骤⑤是在含有Fe3+的溶液里滴加氢氧化钠溶液得到Fe(OH)3红褐色沉淀,发生的离子反应为Fe3++3OH-=Fe(OH)3↓;
(1)结合上述分析可知,操作①、⑤中发生了复分解反应,操作②、③、④中存在氧化还原反应,故答案为:①、⑤;②、③、④;
(2)操作①中得到的白色沉淀为BaSO4,医药上常用作钡餐,用于胃部检查;操作⑤得到的是红褐色Fe(OH)3沉淀,故答案为:BaSO4;钡餐;红褐;
(3)操作④中得到的溶液里含有的金属阳离子有Na+和Fe3+,Na+的检验用焰色反应,Fe3+的检验滴加KSCN溶液,故答案为:Na+;Fe3+;焰色反应、滴加KSCN溶液.
点评 本题以废液处理为载体,考查离子反应、氧化还原反应及离子检验,综合性比较强,但重视的是基础性考查,难度不大,只要基础扎实,并有一定基础的分析问题的能力,定能成功解答.


科目:高中化学 来源: 题型:解答题
 氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是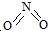 和
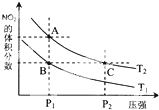
和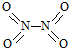 .实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.
.实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
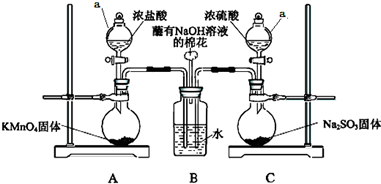 某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验.
某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验内容 | 实验目的 | |
| A | 向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液先变红色后褪色 | 证明有氯水具有酸性 |
| B | 将Cl2通入NaBr溶液中,溶液变黄 | 比较氯气比液溴的氧化性强 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 证明氧化性:Cu2+>Fe3+ |
| D | 向某待测溶液中,加入BaCl2溶液,产生白色沉淀,继续滴加稀盐酸,沉淀不消失 | 证明待测溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )| A. | 等浓度的两种酸其酸性相同 | |
| B. | 两种酸都能与溴水发生加成反应 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 鞣酸能与Fe3+发生显色反应,而莽草酸不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a=1.38 | B. | a=1.31 | C. | b=174 | D. | b=129 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 比较钾、钠:Na、K、H2O | |
| B. | 比较镁、铝:MgCl2溶液、AlCl3溶液、NaOH溶液 | |
| C. | 比较硫、氯:Na2S溶液、NaCl溶液、pH试纸 | |
| D. | 比较溴、碘:溴水、KI淀粉试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
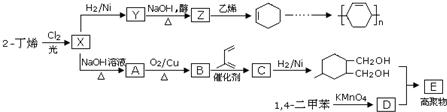
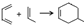 .
.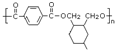 ;甲是A的一种同分异构体,其能实现转化:
;甲是A的一种同分异构体,其能实现转化: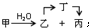 ,甲的名称为乙酸乙酯;
,甲的名称为乙酸乙酯;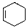 可以合成
可以合成 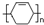 .按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚.
.按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com