
��15�֣���ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪH2��Ϊ����֤��һ��ʵ��ijͬѧ������ͼ��ʾװ�ý���ʵ�飨ʵ��ʱѹǿΪ101 kPa���¶�Ϊ0 �棩��
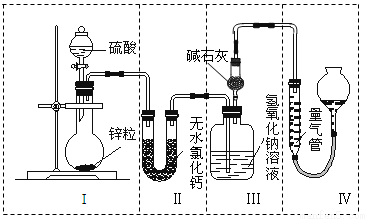
��1��������ƿ�з���0.65 gп������c mol��L��1��H2SO4��Ӧ��Ϊ��֤ʵ����۵Ŀɿ��������ܵ����˹���� ��
A��200 mL B��300 mL C��400 mL
��2����0.65gп����ȫ�ܽ⣬װ�â� ����0.64 g����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3������ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g�����������ռ���V mL���壬���У�a g��65 g��mol��1��2��b g��64 g��mol��1��2+V mL��22400 mL��mol��1��2���õ�ʽ���ݵ�ԭ���� ��
��4��������ƿ��Ͷ��10gп������һ������18 mol��L��1Ũ����10 mL����ַ�Ӧ��п��ʣ�࣬���װ�â� ����3.2 g��������ʵ����̲����������У�m(SO2)/m(H2)= ��������װ�â���ʢ����ˮ�Ȼ��Ƶ�U�ιܣ�m(SO2) / m(H2)����ֵ�� ���ƫ����ƫС������Ӱ�족����
��1��B ��3�֣� ��2��Zn��2H2SO4(Ũ)��ZnSO4��SO2����2H2O��3�֣�
��3��ת�Ƶ����غ� ��3�֣� ��4��20��1 ��3�֣� ƫ��3�֣�
��������
�����������1��Zn+H2SO4��ZnSO4+H2��
1mol 22.4L
0.65g��65g/mol V
���V��0.224L��224ml����ѡB��
��2�����������Ǽ�������������壬��������ϴ��ƿ����˵���������������ɣ���п�����ᷴӦʱ��п����ԭ����������������������ԭΪ��������Zn+2H2SO4��Ũ����ZnSO4+SO2��+2H2O��
��3������������ԭ��Ӧ�е�ʧ����������г�ʽ�ӣ�
��4�����ӵ�������SO2�����������ʵ�����3.2g��64g/mol��0.05mol��Ũ��������ʵ�����0.18mol��
Zn+2H2SO4��Ũ����ZnSO4+SO2��+2H2O
2mol 1mol
0.1mol 0.05mol
������п��Ӧ��ϡ���ᷴӦ�����ʵ�����0.08mol
ʣ��п��������10g��0.05mol��65g/mol��6.75g
�����ʵ�����6.75g��65g/mol��0.1mol
����������������������0.08mol
�������ʵ����̲����������У�m(SO2)/m(H2)��0.05��64��0.08��2��20��1
������ʢ����ˮ�Ȼ��Ƶ�U�ܣ���������е�ˮ������������������Һ������ϴ��ƿ�������������Լ���ʱ������������ʵ�����������m(SO2) / m(H2)����ֵ��ƫ��
���㣺����п��Ũ���ᷴӦ���й��ж������


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�������������������������һ�������¾��ܷ�����Ӧ����
��� | �� | �� | �� |
A | Al | HCl | NaOH |
B | NH3 | O2 | HNO3 |
C | SiO2 | NaOH | HF |
D | SO2 | Ca(OH)2 | NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ̩���н������߶���ѧ���п��Ի�ѧ�Ծ���ѡ�ޣ��������棩 ���ͣ�ѡ����
�����κ�һ��ƽ����ϵ���������´�ʩ��һ����ʹƽ���ƶ�����
A�������¶� B������һ�ַ�Ӧ��
C����ƽ����ϵ����ѹǿ D��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ������������ȷ����
A����ˮ�м��������ѻ����������ú��ϲ���ɫ��dz���²���ɫ��Ϊ�Ϻ�ɫ
B�����ȵ�ͭ˿��������ȼ�գ��������ػ�ɫ����
C������Ȼ��Ʊ�����Һ���������������ͨ��⻯�ص�����Һ�У���Һ����
D���廯����Һ�м����������Ƶ���ˮ���ټ����������Ȼ�̼��Һ�����ú��ϲ���ɫ��dz���²���ɫ��Ϊ�Ⱥ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ӣ���ָ���Ļ�����һ���ܴ����������
A���μ�ʯ����Һ�Ժ�ɫ����Һ��Fe3����NH4����C1����SCN��
B�����д���HCO3������Һ��NH4+��Ca2+��Mg2����I��
C��c(S2��)��0.1 mol��L��1����Һ�У�Na����NH4����ClO����SO42��
D�����д���MnO4������Һ��H+��Mg2+��SO32����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ν��Լ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��8g Na2O2��Na2O��Na2CO3��NaOH�Ĺ��������400g��������Ϊ3.65%������ǡ�÷�Ӧ��������Һ�����յù�������Ϊ
A��16g B��23.4g C��31g D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ν��Լ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����һ�����ʵ���Ũ�ȵ�NaOH��Һʱ�����������ҺŨ��ƫ�͵�ԭ����
A��δϴ���ձ��Ͳ�����
B��ת����Һǰ��Һδ��ȴ������
C������ƿδ����
D������ʱ����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭ����Ҫ���ջ�ͭ����Ҫ�漰���·�Ӧ����2CuFeS2+O2= Cu2S+2FeS+SO2��Cu2S+O2=2Cu+SO2������˵����ȷ����
A���ڷ�Ӧ���У�SO2���������������ǻ�ԭ����
B���ڷ�Ӧ���У�Cu2S������ԭ������Ԫ�ر�����
C���ڷ�Ӧ���У�ÿת��1��2 mol���ӣ���0��2 mol������
D���ڷ�Ӧ���У�ÿ����1��0 molCu2S����4��0 mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ��ѧ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��12�֣�Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС�����������ʵ�����̣��ú�����������ͭ�ĺϽ������ȡ�Ȼ������̷�����(FeSO4��7H2O)�͵������塣
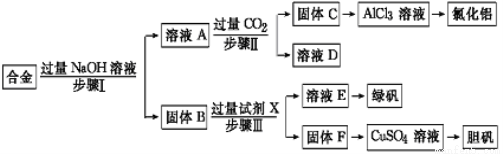
��ش�
��1��д�������Ӧ�����ӷ���ʽ�� ��
��2���Լ�X�� ��������о�����е�ʵ������� ��
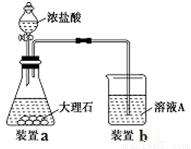
��3�����в����ʱ����С��������ͼ��ʾװ�ü��Լ���ȡCO2�����Ƶõ�����ͨ����ҺA�С�һ��ʱ��۲쵽�ձ��в����İ�ɫ���������١�Ϊ�˱������C���٣��ɲ�ȡ�ĸĽ���ʩ�� ��
��4���ù���F�Ʊ�CuSO4��Һ���������������;����

д��;�����з�Ӧ�����ӷ���ʽ ����ѡ������Ϊ�����;����˵��ѡ������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com