
【题目】按要求填空:
(1)按要求书写下列物质的系统命名:
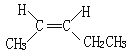
①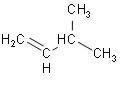 ,将其在催化剂存在下完全与氢气加成所得的产物____;
,将其在催化剂存在下完全与氢气加成所得的产物____;
②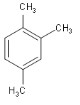 ____。
____。
(2)书写下列物质的结构简式:
①分子式为C5H10的烃存在顺反异构,写出它的顺反两种异构体的结构简式:_____;
②分子式为C9H12的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简式:_____。
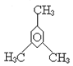
(3)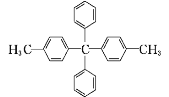 共线的碳原子最多有____个。
共线的碳原子最多有____个。
【答案】2-甲基丁烷 1,2,4-三甲基苯 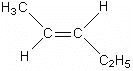 、
、
 4
4
【解析】
(1)①有机物分子中含有碳碳双键,属于烯烃,其名称为3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷;
②编号从小到大,且和最小;
(2)①分子式为C5H10的烃存在顺反异构,说明存在碳碳双键,结构简式为:CH3CH=CHCH2CH3;
②分子式为C9H12的芳香烃,不饱和度为3,苯环上的一溴取代物只有一种,说明苯环上氢等效,满足的只有1,3,5-三甲基苯;
(3)甲烷为正四面体结构,苯环平面结构,相对的碳原子在一条直线上由此分析。
(1)①有机物分子中含有碳碳双键,属于烯烃,其名称为3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷,故答案为:2-甲基丁烷;
②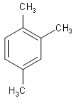 的名称为:1,2,4-三甲基苯;
的名称为:1,2,4-三甲基苯;
(2) ①分子式为C5H10的烃存在顺反异构,说明存在碳碳双键,结构简式为:CH3CH=CHCH2CH3,它的顺反两种异构体的结构简式为: 、
、 ,故答案为:
,故答案为: 、
、 ;
;
②分子式为C9H12的芳香烃,不饱和度为3,苯环上的一溴取代物只有一种,说明苯环上氢等效,满足的只有1,3,5-三甲基苯,结构简式为: ,故答案为:
,故答案为: ;
;
(3)甲烷为正四面体结构,苯环平面结构,相对的碳原子在一条直线上,故该物质共线的碳原子最多有4个,故答案为:4。


科目:高中化学 来源: 题型:
【题目】某种兴奋剂的结构简式如图所示,下列有关该物质的说法正确的是( )
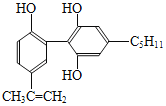
A.该分子中的所有原子有可能共平面
B.该物质与苯酚属于同系物,遇FeCl3溶液显紫色
C.滴入KMnO4(H+)溶液,观察紫色褪去,说明结构中一定存在不饱和碳碳键
D.1mol该物质分别与浓溴水、H2反应时最多消耗的Br2和H2分别为4mol、7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知P4单质的结构如下,P4在 KOH 溶液中的变化是:P4 + 3KOH + 3H2O = 3KH2PO2 + PH3 ↑,下列说法正确的是( )
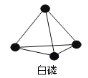
A.产物 PH3分子中所有的原子可能共平面
B.31gP4含有 1.5NA个 P P 键
C.相关元素的电负性大小顺序:P > O > H > K
D.P4中 P 原子为 sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 可以写成
可以写成![]() 。有机物A的结构如下图所示,请回答:
。有机物A的结构如下图所示,请回答:

(1)有机物A分子所含官能团的名称为__________________。
(2)1mol A最多与____mol H2在一定条件下反应可生成环烃B。
(3)有机物A的分子式为_____________________________。
(4)有机物C是A的同分异构体,属于芳香烃,且C在一定条件下可发生聚合反应,生成高分子化合物D。则C的结构简式为______________,D的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列与转化关系,回答有关问题:
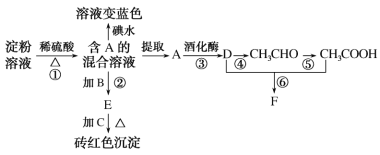
已知:CH3CHO在一定条件下可被氧化为CH3COOH。
(1)A的结构简式为_____,C试剂是_____(填化学式)。
(2)B溶液的作用是_____。
(3)④反应的化学方程式及反应类型分别为_____。
(4)由图示转化关系可知淀粉_____(填“部分水解”或“完全水解”)。某同学取图中混合液E,加入碘水,溶液不变蓝色,______(填“能”或“不能”)说明淀粉水解完全,原因是_____。
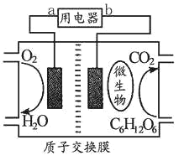
(5)以葡萄糖为燃料的微生物燃料电池如图所示,该电池_____(填“能”或“不能”)在高温下工作,酸性条件下负极电极反应的方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在医药工业中,有机物 G是一种合成药物的中间体 ,其合成路线如图所示 :
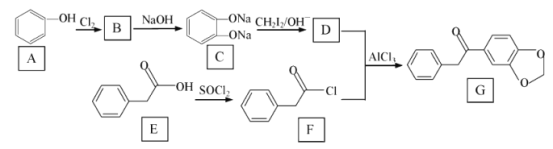
已知:R1ONa+R2X→R1OR2+NaX(R1与 R2代表苯环或烃基、X 代表卤素原子)
RCOOH+SOCl2(液体)→RCOCl+HCl↑+SO2↑
回答下列问题:
(1)A 与C在水中溶解度更大的是 _________ , G 中官能团的名称是 ___________。
(2)E→F 的有机反应类型是 ________ ,F 的分子式为______________。
(3)由A→B反应的化学方程式为 ___________________。
(4)物质D的结构简式为 _________________。
(5)B→C 反应中加入NaOH 的作用是________________。
(6)写出一种符合下列条件的G的同分异构体 _________________ 。
①与G的苯环数相同;②核磁共振氢谱有5 个峰;③能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:乙二酸(HOOC—COOH,可简写为H2C2O4),俗称草酸,157℃时开始分解。
(1)探究草酸的酸性
25℃ H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3 K1=4.5×10-7,K2=4.7×10-11
下列化学方程式可能正确的是___。
A.H2C2O4+![]() =
=![]() +
+![]() B.
B.![]() +
+![]() =
=![]() +
+![]()
C.2![]() +CO2+H2O=2
+CO2+H2O=2![]() +
+![]() D.H2C2O4+
D.H2C2O4+![]() =
=![]() +H2O+CO2↑
+H2O+CO2↑
(2)探究草酸分解产物
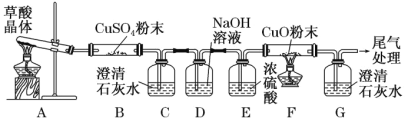
实验中观察到 B 中 CuSO4 粉末变蓝,C 中澄清石灰水变浑浊,D 的作用是 ___, 证明有 CO 气体生成的现象是______。
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入 4 mL 0.01 mol·L-1 酸性 KMnO4 溶液和 2 mL 0.1 mol·L-1H2C2O4 溶液,再向乙试管中加入一粒黄豆大的 MnSO4 固体,摇匀。填写表格:
反应现象 | ①_______ |
实验结论 | ②______ |
试管中发生反应的离子方程式 | ③______ |
(4)用酸性 KMnO4 溶液滴定 Na2C2O4,求算 Na2C2O4 的纯度。
实验步骤:准确称取 2.0 g Na2C2O4 固体,配成 100 mL 溶液;取出 20.00 mL 于锥形瓶
①KMnO4 溶液应装在_________ 滴定管中。(填“酸式”或“碱式”)
②Na2C2O4 的纯度是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。用甲烷制水煤气(CO、H2),再合成甲醇可以代替日益供应紧张的燃油。下面是产生水煤气的几种方法:
①CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1=+206.2kJ·mol-1
②CH4(g)+![]() O2(g)=CO(g)+2H2(g) ΔH2=-35.4kJ·mol-1
O2(g)=CO(g)+2H2(g) ΔH2=-35.4kJ·mol-1
③CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH3=+165.0kJ·mol-1
(1)CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为__。
(2)从原料、能源利用的角度,分析以上三个反应,作为合成甲醇更适宜的是反应__(填序号)。
(3)也可将CH4设计成燃料电池,来解决能源问题,如图装置所示。持续通入甲烷,在标准状况下,消耗甲烷VL。
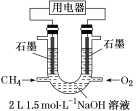
①0<V≤33.6L时,负极电极反应式为__。
②33.6L<V≤67.2L时,电池总反应方程式为__。
③V=44.8L时,溶液中离子浓度大小关系为__。
(4)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量。某小组研究在上述温度下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达到平衡时体系能量的变化/kJ | ||
N2 | H2 | NH3 | |||
Ⅰ | 1 | 4 | 0 | t1 | 放出热量:36.88 |
Ⅱ | 2 | 8 | 0 | t2 | 放出热量:Q |
①容器Ⅰ中,0~t1时间的平均反应速率v(H2)=__。
②下列叙述正确的是__(填字母)。
a.平衡时,两容器中H2的体积分数相等
b.容器Ⅱ中反应达到平衡状态时,Q>73.76
c.反应开始时,两容器中反应的化学反应速率相等
d.平衡时,容器中N2的转化率:Ⅰ<Ⅱ
e.两容器达到平衡时所用时间:t1>t2
(5)如图是在反应器中将N2和H2按物质的量之比为1∶3充入后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的体积分数随压强的变化曲线。

①曲线a对应的温度是__。
②图中M、N、Q点平衡常数K的大小关系是__。
③M点对应的H2转化率是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用甲苯合成苯甲醛的一种合成路线如下图所示。下列说法中正确的是( )
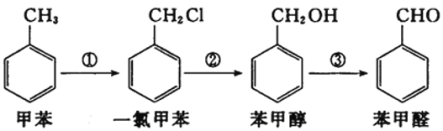
A.甲苯的一氯取代物有5种B.苯甲醇与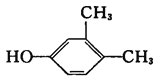 互为同系物
互为同系物
C.苯甲醛既有氧化性又有还原性D.①②③的反应类型相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com