
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:

(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
0~50s内的平均反应速率v(N2)=_________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。![]() 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1mol NH3过程中___(填“吸收”或“放出”)的能量为____,反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1mol NH3过程中___(填“吸收”或“放出”)的能量为____,反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)为加快反应速率,可以采取的措施是_______
a.降低温度
b.增大压强
c.恒容时充入He气
d.恒压时充入He气
e.及时分离NH3
【答案】3X+Y2Z 1.2×103mol/(L·s) 放出 46kJ 18.4 b
【解析】
(1)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;
(2)根据![]() =
=![]() 计算;
计算;
(3)形成化学键放出能量,断裂化合价吸收能量;
(4)根据影响反应速率的因素分析;
(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为3X+Y2Z;
(2)0~50s内,NH3物质的量变化为0.24mol,根据方程式可知,N2物质的量变化为0.12mol,![]() (Z)=
(Z)=![]() =
=![]() 1.2×103mol/(L·s);
1.2×103mol/(L·s);
(3)断裂1mol![]() 吸收946kJ的能量,断裂1mol H-H键吸能量436kJ,形成1mo N-H键放出能量391kJ,根据方程式3H2+N22NH3,生成2mol氨气,断键吸收的能量是946kJ+ 436kJ×3=2254 kJ,成键放出的能量是391kJ×6=2346 kJ,则生成1mol NH3过程中放出的能量为
吸收946kJ的能量,断裂1mol H-H键吸能量436kJ,形成1mo N-H键放出能量391kJ,根据方程式3H2+N22NH3,生成2mol氨气,断键吸收的能量是946kJ+ 436kJ×3=2254 kJ,成键放出的能量是391kJ×6=2346 kJ,则生成1mol NH3过程中放出的能量为![]() =46kJ;反应达到(2)中的平衡状态时生成0.4mol氨气,所以放出的能量是46kJ×0.4=18.4kJ;
=46kJ;反应达到(2)中的平衡状态时生成0.4mol氨气,所以放出的能量是46kJ×0.4=18.4kJ;
(4) a.降低温度,反应速率减慢,故不选a;
b.增大压强,体积减小浓度增大,反应速率加快,故选b;
c.恒容时充入He气,反应物浓度不变,反应速率不变,故不选c;
d.恒压时充入He气,容器体积增大,反应物浓度减小,反应速率减慢,故不选d;
e.及时分离NH3,浓度减小,反应速率减慢,故不选e。


科目:高中化学 来源: 题型:
【题目】已知单质铜与稀硝酸的反应为3Cu+8HNO3=2NO↑+4H2O+3Cu(NO3)2(Cu的相对原子质量为64)。现把19.2 g Cu放入200 mL 5 mol·L-1硝酸中,充分反应,问:
(1)参加反应的硝酸的物质的量为多少?______________
(2)在标准状况下产生的气体的体积为多少?____________
(3生成水的分子数为多少?___________
(4)若反应前后溶液的体积不变,则生成Cu(NO3)2的物质的量浓度为多少?__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是常温下几种常见弱酸的电离平衡常数:
弱酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | K=1.6×10-5 |
H2C2O4 | H2C2O4 HC2O4- | K1=5.9×10-2 K2=6.4×10-5 |
H2CO3 | H2CO3 | K1=4.4×10-7 K2=5.6×10-11 |
H2S | H2S | K1=9.1×10-8K2=1.1×10-15 |
回答下列问题:
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,则此时溶液中c(OH-)为_______mol/L;此时温度__________25 ℃(填“大于”,“小于”或“等于”),若温度不变,滴入稀硫酸使c(H+)=5.0×10-6mol/L,则由水电离出的c(H+)为______mol/L。
(2)下列四种离子结合H+能力最强的是______。
A.HCO3- B. C2O42- C. S2- D.CH3COO-
(3)该温度下1.0 mol·L-1的CH3COOH溶液中的c(H+)=_____span> mol·L-1
(4)常温下,加水稀释0.1 mol·L-1的H2C2O4溶液,下列说法正确的是(______)
A.溶液中n(H+)×n(OH-)保持不变
B.溶液中水电离的c(H+)×c(OH-)保持不变
C.溶液中c(HC2O4-)/c(H2C2O4)保持不变
D.溶液中c(OH-)增大
(5)将CH3COOH溶液加入少量Na2CO3溶液中,反应的离子方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用如图所示装置探究金属的腐蚀与防护,下列有关说法错误的是

A. 图①,放置于干燥空气中的铁钉不易生锈
B. 图②,用酒精灯加热具支试管,可以更快更清晰地观察到液柱上升
C. 图③,利用了外加电流的阴极保护法保护钢闸门不被腐蚀
D. 图④,利用了牺牲阳极的阴极保护法保护钢铁输水管不被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新泽茉莉醛是一种名贵的香料,合成过程中还能得到一种PC树脂,其合成路线如图。
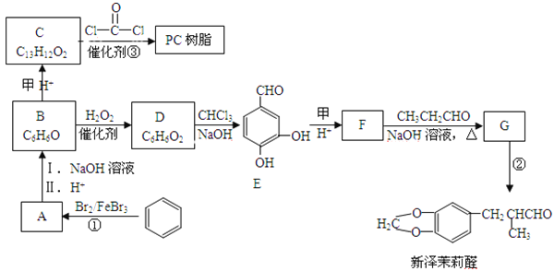
已知:①RCHO+R′CH2CHO![]()
![]() +H2O
+H2O
②RCHO+HOCH2CH2OH![]()
![]() +H2O
+H2O
③![]() +2ROH
+2ROH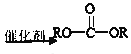 +HCl
+HCl
(1)E的含氧官能团名称是_________,E分子中共面原子数目最多为___________。
(2)写出反应①的化学方程式_________________________________。
(3)写出符合下列条件并与化合物E互为同分异构体的有机物结构简式____________。
a.能与浓溴水产生白色沉淀
b.能与![]() 溶液反应产生气体
溶液反应产生气体
c.苯环上一氯代物有两种
(4)反应②的反应类型是_______。
(5)已知甲的相对分子质量为30,写出甲和G的结构简式____________、___________。
(6)已知化合物C的核磁共振氢谱有四种峰,写出反应③的化学方程式______________。
(7)结合已知①,以乙醇和苯甲醛(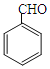 )为原料,选用必要的无机试剂合成
)为原料,选用必要的无机试剂合成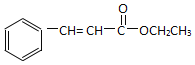 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)______________________________。
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃 A 是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A 还是一种植物生长调节剂,A 可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据图像回答下列问题:
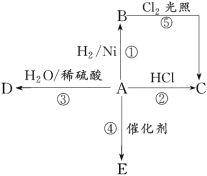
(1)写出 A和D 的结构简式:A________,D________。
(2)写出②、⑤两步反应的化学方程式,并注明反应类型:
②________,反应类型________。
⑤________,反应类型________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在固定体积的密闭容器中进行可逆反应:![]() 。该可逆反应达到平衡的标志是
。该可逆反应达到平衡的标志是
A.![]()
B.单位时间生成![]() 的同时生成
的同时生成![]()
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.9 g D2O中含有的电子数为5NA
B.46 g NO2和N2O4混合气体中含有原子数为3NA
C.1 mol C2H6分子中含共价键总数为6NA
D.7.1 g C12与足量NaOH溶液反应,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是一种重要的有机化工原料,其结构简式为![]() ,它一般不可能具有的性质是
,它一般不可能具有的性质是
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D. 能发生加成反应,在一定条件下可与4倍物质的量的氢气加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com