

���� ��1������װ��ͼ��֪�������ƣ����ݲ���������ȴЧ�����жϽ�ˮ�ڣ�
��2���ٸ��ݳ��˵IJ���Ҫ���֪�����˲������ڽ�״������Ҳ�������ڿ���̫С�ij������ݴ˴��⣻
�ڸ��ݳ��˲����Ĺ淶Ҫ���֪���ڴ�װ��ʱ��ֽӦ��©���ھ���С�����ܸ�ס����С�ף���ͼ2����װ����©������б��Ӧ��������ƿ��֧�ܿڣ�ͬʱ��ȫƿ�е��ܲ���̫�����������������������˵õ�����ҺӦ������ƿ���Ͽڵ�����������Ϻ�Ӧ�Ȳ������ӳ����ú�����ƿ����Ƥ�ܣ��ٹ�ˮ��ͷ���Է��������ݴ˴��⣻
��3������Ԫ���غ�͵���غ���д���ӷ���ʽ��
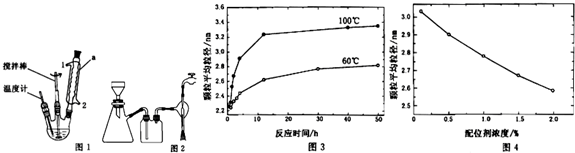
��4��A������ͼ3��֪���ı䷴Ӧ�¶Ⱥͷ�Ӧʱ�䣬���Եõ�ƽ��������ͬ��CdSe��������
B����ͼ3��ʾ�������¶��£�100�桢60�淴Ӧ�����¶��ɵõ�2.7nm��CdSe��������
C������ͼ3��֪����������������ʱ���¶�Խ�õ���CdSe������Խ��
D������ͼ3��֪����60��ò���3.0nm��CdSe�����������������Ҫ�õ�3.0nm��CdSe���������ɳ��Խ�����λ��Ũ�ȵķ�����
��� �⣺��1������װ��ͼ��֪����a������Ϊ�����ܣ����ݲ���������ȴЧ���ÿ�֪����ˮ��ӦΪ2���ʴ�Ϊ�������ܣ�2��
��2���ٸ��ݳ��˵IJ���Ҫ���֪�����˲������ڽ�״������Ҳ�������ڿ���̫С�ij��������Է���CdSe���������˲��ó��˵ķ�����
�ʴ�Ϊ�����˲������ڽ�״���������̫С�ij�����
�ڸ��ݳ��˲����Ĺ淶Ҫ���֪��A���ڴ�װ��ʱ��ֽӦ��©���ھ���С�����ܸ�ס����С�ף���A��ȷ��
B����ͼ2����װ��������������©������б��Ӧ��������ƿ��֧�ܿڣ�ͬʱ��ȫƿ�е��ܲ���̫������B����
C�����˵õ�����ҺӦ������ƿ���Ͽڵ�������C����
D��������Ϻ�Ӧ�Ȳ������ӳ����ú�����ƿ����Ƥ�ܣ��ٹ�ˮ��ͷ���Է���������D��ȷ��
��ѡAD��
��3����SeSO32-�ڼ�������������HSe-����Ӧ�����ӷ���ʽΪSeSO32-+OH-=HSe-+SO42-����HSe-��Cd2+��Ӧ����CdSe����Ӧ�����ӷ���ʽΪHSe-+OH-+Cd2+=CdSe+H2O��
�ʴ�Ϊ��OH-��SO42-��HSe-+OH-+Cd2+=CdSe+H2O��
��4��A������ͼ3��֪���ı䷴Ӧ�¶Ⱥͷ�Ӧʱ�䣬���Եõ�ƽ��������ͬ��CdSe����������A��ȷ��
B����ͼ3��ʾ�������¶��£�100�桢60�淴Ӧ�����¶��ɵõ�2.7nm��CdSe����������B����
C������ͼ3��֪����������������ʱ���¶�Խ�õ���CdSe������Խ��C����
D������ͼ3��֪����60��ò���3.0nm��CdSe�����������������Ҫ�õ�3.0nm��CdSe���������ɳ��Խ�����λ��Ũ�ȵķ�������D��ȷ��
��ѡAD��
���� ���⿼��ʵ������������������Ʊ��ȣ�Ϊ��Ƶ���㣬�������������Ϣ�ǽⱾ��ؼ���ע������ͼ����Ϣ�Ļ�ȡ��Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ͼ��a����ʾ��ʵ�飺���ݼ����ƣ�G����ָ��ƫת�ķ���Ƚ�Zn��Cu�Ľ��������� | |
| B�� | ͼ��b����ʾ��ʵ�飺����С�Թ���Һ��ı仯�ж������������ⸯʴ | |
| C�� | ͼ��c����ʾ��ʵ�飺�����¶ȼƶ����ı仯��ϡ�����ϡNaOH��Һ��Ӧ�ⶨ�к��� | |
| D�� | ͼ��d����ʾ��ʵ�飺��������ƿ��������ɫ�ı仯�ж�2NO2��g��?N2O4��g���Ƿ��ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����Fe2+��I-��Br -����Һͨ��������������Һ�����������ӵ����ʵ����ı仯��ͼ��ʾ������˵������ȷ���ǣ�������
�����Fe2+��I-��Br -����Һͨ��������������Һ�����������ӵ����ʵ����ı仯��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | �߶����Fe2+�ı仯��� | B�� | �߶����Br -�ı仯��� | ||
| C�� | ԭ�����Һ��n��FeBr2��=4mol | D�� | a��ֵ����6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 0.082 | B�� | 0.072 | C�� | 0.072MPa-1 | D�� | 0.082 MPa-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com