
【题目】用如图装置探究NH3和CuSO4溶液的反应。
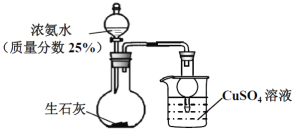
(1)上述制备NH3的实验中,烧瓶中反应涉及到多个平衡的移动:NH3+H2O![]() NH3H2O、____________、_________________(在列举其中的两个平衡,可写化学用语也可文字表述)。
NH3H2O、____________、_________________(在列举其中的两个平衡,可写化学用语也可文字表述)。
(2) 制备100mL25%氨水(ρ=0.905gcm-3),理论上需要标准状况下氨气______L(小数点后保留一位)。
(3) 上述实验开始后,烧杯内的溶液__________________________,而达到防止倒吸的目的。
(4)NH3通入CuSO4溶液中,产生蓝色沉淀,写出该反应的离子方程式。_______________________。继续通氨气至过量,沉淀消失得到深蓝色[Cu(NH3)4]2+溶液。发生如下反应:2NH4+(aq)+Cu(OH)2(s)+2NH3(aq)![]() [Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)。
[Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)。
①该反应平衡常数的表达式K=___________________________。
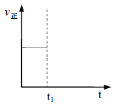
②t1时改变条件,一段时间后达到新平衡,此时反应K增大。在下图中画出该过程中v正的变化___________________。
③向上述铜氨溶液中加水稀释,出现蓝色沉淀。原因是:________________________________。
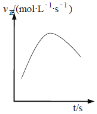
④在绝热密闭容器中,加入NH4+(aq)、Cu(OH)2和NH3(aq)进行上述反应,v正随时间的变化如下图所示,v正先增大后减小的原因__________________________________。
【答案】NH3H2O![]() NH4++OH- NH3(g)
NH4++OH- NH3(g)![]() NH3(aq)(或氨气的溶解平衡) Ca(OH)2(s)
NH3(aq)(或氨气的溶解平衡) Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq)(或Ca(OH)2 的溶解平衡) 29.8 进入干燥管后,又回落至烧杯,如此反复进行 Cu2++2NH3H2O→ Cu(OH)2↓+2NH4+ [[Cu(NH3)4]2+]/[ NH3]2[NH4+] 2
Ca2+(aq)+2OH-(aq)(或Ca(OH)2 的溶解平衡) 29.8 进入干燥管后,又回落至烧杯,如此反复进行 Cu2++2NH3H2O→ Cu(OH)2↓+2NH4+ [[Cu(NH3)4]2+]/[ NH3]2[NH4+] 2  加水,反应物、生成物浓度均降低,但反应物降低更多,平衡左移,生成了更多的Cu(OH)2(加水稀释后c[Cu(NH3)4]2+/c2 (NH3) c2 (NH4+) 会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀 该反应是放热反应,反应放出的热使容器内温度升高,v正 增大;随着反应的进行,反应物浓度减小,v正 减小
加水,反应物、生成物浓度均降低,但反应物降低更多,平衡左移,生成了更多的Cu(OH)2(加水稀释后c[Cu(NH3)4]2+/c2 (NH3) c2 (NH4+) 会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀 该反应是放热反应,反应放出的热使容器内温度升高,v正 增大;随着反应的进行,反应物浓度减小,v正 减小
【解析】
(1) 制备NH3的实验中,存在着NH3+H2O![]() NH3H2O、NH3的溶解平衡和Ca(OH)2 的溶解平衡三个平衡过程;
NH3H2O、NH3的溶解平衡和Ca(OH)2 的溶解平衡三个平衡过程;
(2) 氨水是指NH3的水溶液,不是NH3·H2O的水溶液,所以要以NH3为标准计算. n(NH3)= ![]() =1.33 mol;
=1.33 mol;
(3) 实验开始后,烧杯内的溶液进入干燥管后,又回落至烧杯,如此反复进行,而达到防止倒吸的目的;
(4) NH3通入CuSO4溶液中和水反应生成NH3H2O,NH3H2O电离出OH-,从而生成蓝色沉淀Cu(OH)2;
①反应2NH4+(aq)+Cu(OH)2(s)+2NH3(aq)![]() [Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0),平衡常数的表达式K=
[Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0),平衡常数的表达式K=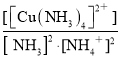 ;
;
②反应2NH4+(aq)+Cu(OH)2(s)+2NH3(aq)![]() [Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)是放热反应,降温可以使K增大,正逆反应速率都减少;
[Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)是放热反应,降温可以使K增大,正逆反应速率都减少;
③向上述铜氨溶液中加水稀释,出现蓝色沉淀。原因是:加水,反应物、生成物浓度均降低,但反应物降低更多,平衡左移,生成了更多的Cu(OH)2(加水稀释后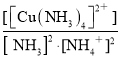 会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀;
会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀;
④在绝热密闭容器中,加入NH4+(aq)、Cu(OH)2和NH3(aq)进行上述反应,v正先增大后减小的原因,温度升高反应速度加快,反应物浓度降低反应速率又会减慢。
(1) 制备NH3的实验中,存在着NH3+H2O![]() NH3H2O、NH3的溶解平衡和Ca(OH)2 的溶解平衡三个平衡过程,故答案为:NH3H2O
NH3H2O、NH3的溶解平衡和Ca(OH)2 的溶解平衡三个平衡过程,故答案为:NH3H2O![]() NH4++OH- NH3(g)
NH4++OH- NH3(g)![]() NH3(aq)(或氨气的溶解平衡)、Ca(OH)2(s)
NH3(aq)(或氨气的溶解平衡)、Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq)(或Ca(OH)2 的溶解平衡);
Ca2+(aq)+2OH-(aq)(或Ca(OH)2 的溶解平衡);
(2) 氨水是指NH3的水溶液,不是NH3·H2O的水溶液,所以要以NH3为标准计算. n(NH3)= ![]() =1.33 mol,标准状况下体积为1.33mol×22.4L/mol=29.8L;
=1.33 mol,标准状况下体积为1.33mol×22.4L/mol=29.8L;
(3) 实验开始后,烧杯内的溶液进入干燥管后,又回落至烧杯,如此反复进行,而达到防止倒吸的目的;
(4) NH3通入CuSO4溶液中和水反应生成NH3H2O,NH3H2O电离出OH-,从而生成蓝色沉淀Cu(OH)2,该反应的离子方程式为:Cu2++2NH3H2O→ Cu(OH)2↓+2NH4+;
①反应2NH4+(aq)+Cu(OH)2(s)+2NH3(aq)![]() [Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0),平衡常数的表达式K=
[Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0),平衡常数的表达式K=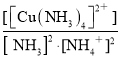 ;
;
②反应2NH4+(aq)+Cu(OH)2(s)+2NH3(aq)![]() [Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)是放热反应,降温可以使K增大,正逆反应速率都减少,画出该过程中v正的变化为:
[Cu(NH3)4]2+(aq)(铜氨溶液)+2H2O+Q(Q>0)是放热反应,降温可以使K增大,正逆反应速率都减少,画出该过程中v正的变化为: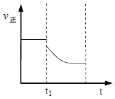 ;
;
③向上述铜氨溶液中加水稀释,出现蓝色沉淀。原因是:加水,反应物、生成物浓度均降低,但反应物降低更多,平衡左移,生成了更多的Cu(OH)2(加水稀释后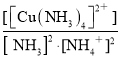 会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀;
会大于该温度下的K,平衡左移,生成了 更多的Cu(OH)2,得到蓝色沉淀;
④在绝热密闭容器中,加入NH4+(aq)、Cu(OH)2和NH3(aq)进行上述反应,v正先增大后减小的原因,温度升高反应速度加快,反应物浓度降低反应速率又会减慢,故原因是:该反应是放热反应,反应放出的热使容器内温度升高,v正 增大;随着反应的进行,反应物浓度减小,v正 减小。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g);△H<0,下列研究目的和示意图相符的是
A | B | C | D | |
研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 增加H2的浓度对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①稀硫酸 ②小苏打 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液 ⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______。
(4)能导电的物质序号为_______________。
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)___________________________。
(6)实验室用⑤制备胶体的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为7:17,X与W同主族,Y的原子序数是W和X的原子序数之和的一半,含Z元素的物质在焰色反应实验中的焰色为黄色。下列判断正确的是
A.金属性:Y>ZB.非金属性:W>X
C.原子半径:W>Y>ZD.氢化物的热稳定性:X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成了一种新化合物(如图所示),其中X、Y是第三周期的非金属元素,各原子均满足8电子稳定结构。
完成下列填空:

(1)硅原子最外电子层有________种运动状态不同的电子,占据______个轨道。
(2)由题意可推知Y是Cl,推得此结论的依据是__________________。X和Si之间共用电子对偏离________。
(3)SiCl4和CCl4分子空间结构相同,则SiCl4中键角是_________。请说明SiCl4和CCl4沸点高低的理由。__________________________________________。
(4)黄磷(P4)与过量浓NaOH溶液反应,产生PH3和次磷酸钠(NaH2PO2),补全并配平该反应的化学方程式,标出电子转移的数目和方向:_____P4+_____NaOH+_________→_____PH3↑+_____NaH2PO2,____________________.其中氧化剂和还原剂质量比为________。根据题意可判断H3PO2是________元酸(填“一”、“二”或“三”)。
(5)已知磷酸二氢钠(NaH2PO4)溶液呈酸性,该溶液中含磷元素的离子浓度由大到小的顺序是:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。回答下列问题
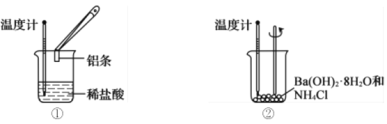
(1)装置①中反应物的总能量比生成物的总能量________(填标号)。
a.高 b.低 c.相等
(2)装置②中反应后溶液的温度__________(填标号)。
a.升高 b.降低 c.不变
(3)已知断裂1mo1共价键需要吸收的能量分别为 H —H :436kJ,I —I :151kJ,H— I :299kJ。则反应 H2+I2 = 2HI的能量变化为______(填标号)。
a.无能量变化 b.吸热 c.放热
(4)碱金属单质在空气中燃烧的产物与碱金属的活动性有关。锂单质在空气中燃烧得到的产物的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W、Q五种元素,它们的核电荷数依次增大,且都小于20,其中X为非金属元素。X和Q属于同一族,它们原子的最外层电子排布式为ns1;Y和W也属于同一族,它们原子的最外层的p能级电子数是s能级电子数的两倍;Z原子最外层上电子数等于W原子最外层上电子数的一半。请回答下列问题:
(1)X、Y可形成一种绿色氧化剂A,则A为__(“极性分子”或“非极性分子”);试写出Cu、稀硫酸与A反应制备CuSO4的离子方程式___。
(2)由这5种元素组成的一种化合物是__(填化学式),该物质主要用途是__,并解释其原理___。
(3)在第四周期中,与Z元素原子未成对电子数相同的金属元素有___种,该元素氯化物的二聚分子结构如图所示,在此化合物中Z原子的杂化类型为___,该化合物在熔融状态下___导电(“能”或“不能”)。
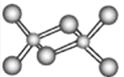
(4)分子WY2、WY3的键角相比,更大的是___(填化学式),写出两种与WY3互为等电子体的微粒___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,通常采用电解法处理酸性废水中的![]() ,装置示意图如图所示。下列说法正确的是
,装置示意图如图所示。下列说法正确的是
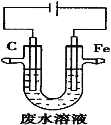
A.石墨极上发生氧化反应
B.阳极的电极反应式为![]()
C.除去![]() 的反应:
的反应:![]()
D.随着电解的进行,石墨极附近电解质溶液的pH会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以工业废铁和硫酸铵为原料可以制取![]() 和硫酸铁铵,其制备流程图如下,请根据题意完成下列填空:
和硫酸铁铵,其制备流程图如下,请根据题意完成下列填空:
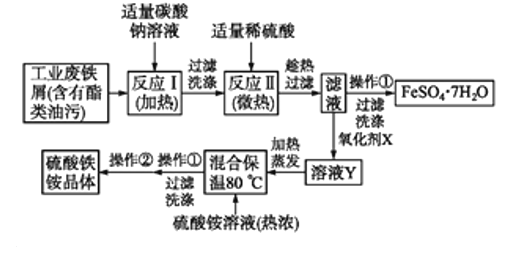
![]() 碳酸钠溶液能除去酯类油污,其原因是
碳酸钠溶液能除去酯类油污,其原因是![]() 用离子方程式表示
用离子方程式表示![]() ______;反应Ⅰ需要加热数分钟,其原因是______.
______;反应Ⅰ需要加热数分钟,其原因是______.
![]() 废铁屑中含氧化铁,无需在制备前除去,其理由是
废铁屑中含氧化铁,无需在制备前除去,其理由是![]() 用离子方程式回答
用离子方程式回答![]() ______;判断反应Ⅱ完全反应的现象是______.
______;判断反应Ⅱ完全反应的现象是______.
![]() 下列物质中最适合的氧化剂X是______.
下列物质中最适合的氧化剂X是______.
![]()
![]()
![]()
![]()
![]() 加热蒸发溶液Y之前,需取少量的溶液来检验
加热蒸发溶液Y之前,需取少量的溶液来检验![]() 是否已全部被氧化,则所加试剂为______;判断能否用酸性
是否已全部被氧化,则所加试剂为______;判断能否用酸性![]() 溶液来代替,并说明其理由______.
溶液来代替,并说明其理由______.
![]() 操作
操作![]() 的名称是______;检验硫酸铁铵中
的名称是______;检验硫酸铁铵中![]() 的方法是______.
的方法是______.
![]() 称取
称取![]() 制得的硫酸铁铵晶体,将其溶于水配制成100mL溶液,分成两等份,向其中一份溶液中加入足量NaOH溶液,过滤、洗涤、干燥后得到
制得的硫酸铁铵晶体,将其溶于水配制成100mL溶液,分成两等份,向其中一份溶液中加入足量NaOH溶液,过滤、洗涤、干燥后得到![]() 沉淀;向另一份溶液中加入
沉淀;向另一份溶液中加入![]() 溶液,恰好完全反应.则该硫酸铁铵晶体的化学式为______.
溶液,恰好完全反应.则该硫酸铁铵晶体的化学式为______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com