
【题目】下列各组混合物能用分液漏斗分离的是( )
A. 四氯化碳和水 B. 汽油和食用油
C. 浓硫酸和浓硝酸 D. 酒精和水
科目:高中化学 来源: 题型:
【题目】用一种试剂将下列各组物质鉴别开。
(1)![]() 和
和![]() :_________________________
:_________________________
(2) ![]() ,
,![]() 和C6H12(已烯):_________________
和C6H12(已烯):_________________
(3) ![]() ,CCl4和乙醇_______________________
,CCl4和乙醇_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a,将其全部投入50mL bmol·L-1的硝酸溶液中,加热使其充分反应(假充NO是唯一的还原产物)。下列说法正确的是
A. 若金属有剩余,反应中转移的电子数目为2yNA
B. 若金属全部溶解,则溶液中一定含有Fe3+
C. 若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D. 当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1- a/3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是
①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
②S ![]() SO3
SO3 ![]() H2SO4
H2SO4
③饱和NaCl(aq)![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe2O3 ![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
⑤MgCl2(aq)![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO
A. ②③④ B. ①④⑤ C. ②④⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟是一种卤族元素。但它与其他卤素在单质和化合物的制备与性质上存在较明显的差异
(1)研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在423 K的温度下制备F2的化学方程式:____________________。
(2)现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
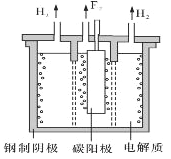
①已知KHF2是一种酸式盐,写出阴极上发生的电极反应式______________。
②电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是____________ 。
③HF的水溶液能用于蚀刻玻璃,其化学反应方程式为:_____________________。
④已知25℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。某pH=2的氢氟酸溶液,由水电离出的c(H+)=_________mol/L;若将0.01 mol/L HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度大小关系为:__________________。
⑤又已知25℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1L0.2 mol/L HF溶液中加入1L0.2 mol/L CaCl2溶液,____________(填“是”、“否”) 有沉淀产生,并通过列式计算说明__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节能减排可以改善环境质量。下述做法正确的是( )
A. 以煤作为主要生活燃料 B. 利用太阳能、风能等替代化石能源
C. 鼓励人们购买和使用汽车 D. 大量使用含磷洗衣粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 化学反应中需要加热的反应一定是吸热反应
B. 化学反应中不需要加热的反应一定是放热反应
C. 熵增加且吸热的反应一定是自发反应
D. 化学反应总是伴随着物质变化和能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O===Fe(OH)2↓+2HClO
B. NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH--===BaCO3↓+H2O
C. 在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3===2FeO![]() +3Cl-+H2O+4H+
+3Cl-+H2O+4H+
D. 用铜作电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com