
| A. | OH-的物质的量 | B. | c(H+) c(OH-) | C. | c(NH4+) | D. | c(OH-) |
分析 稀释氨水溶液过程中,一水合氨是弱电解质,加水稀释促进一水合氨电离,导致铵根离子、氢氧根离子个数增大,但其浓度减小,一水合氨分子个数减小,溶液体积增大,所以一水合氨浓度减小.
解答 解:A、稀释氨水过程中,促进一水合氨电离,溶液中氢氧根离子个数增多,所以OH-的物质的量始终保持增大趋势,故A正确;
B、c(H+) c(OH-)是温度的函数,所以加水稀释Kw不变,故B错误;
C、稀释氨水过程中,促进一水合氨电离,溶液中铵根离子个数增多,但溶液体积增大倍数大于铵根离子物质的量增大倍数,所以铵根离子浓度减小,故C错误;
D、稀释氨水过程中,促进一水合氨电离,溶液中氢氧根离子个数增多,但溶液体积增大倍数大于氢氧根离子物质的量增大倍数,所以氢氧根离子浓度减小,故D错误;
故选A.
点评 本题考查了弱电解质电离,明确弱电解质电离特点是解本题关键,注意稀释过程中,虽然促进一水合氨电离,但溶液体积增大倍数要远远超过铵根离子、氢氧根离子增大倍数,为易错点.


科目:高中化学 来源: 题型:实验题
| 活性炭/mol | NO/mol | A/mol | B/mol | ρ/Mpa | |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 | ρ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{44}$ mol-1 | B. | $\frac{x}{22}$ mol-1 | C. | $\frac{3x}{44}$ mol-1 | D. | $\frac{44x}{3}$ mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强,化学平衡不一定移动 | |
| B. | 通入氦气,化学平衡一定不发生移动 | |
| C. | 增加X或Y的物质的量,化学平衡一定发生移动 | |
| D. | 其它条件不变,升高温度,化学平衡一定发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
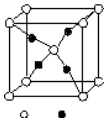 周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题;
周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com