
【题目】CPAE是蜂胶的主要活性成分,它由咖啡酸合成,合成过程如下.下列说法不正确的是( )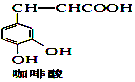 +
+ ![]() →
→ 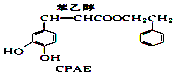 +H2O.
+H2O.
A.1molCPAE和1mol咖啡酸分别与足量的NaOH溶液反应,均最多消耗3molNaOH
B.与苯乙醇互为同分异构体的酚类物质共有9种
C.FeCl3溶液可区别咖啡酸和CPAE
D.咖啡酸可发生聚合反应,并且其分子中含有3种官能团
【答案】C
【解析】A.CPAE中酚羟基、酯基水解生成的羧基能和NaOH溶液反应,咖啡酸中酚羟基和羧基都能和NaOH溶液反应,1molCPAE和1mol咖啡酸分别与足量的NaOH溶液反应,均最多消耗3molNaOH,故A不符合题意;
B.与苯乙醇互为同分异构体的酚类物质,含酚﹣OH、乙基(或2个甲基),含酚﹣OH、乙基存在邻、间、对三种,两个甲基处于邻位的酚2种,两个甲基处于间位的有3种,两个甲基处于对位的有1种,共9种,故B不符合题意;
C.CPAE和咖啡酸中都含有酚羟基,都与氯化铁发生显色反应,所以不能用氯化铁溶液鉴别,故C符合题意;
D.咖啡酸中含有碳碳双键,具有烯烃性质,在一定条件下能发生加聚反应,该分子中含有酚羟基、碳碳双键和羧基三种官能团,故D不符合题意;
所以答案是:C.
【考点精析】解答此题的关键在于理解有机物的结构和性质的相关知识,掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生反应X(g)+2Y(g)![]() 3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
A. 容器内气体的压强不再发生变化,说明反应达到平衡状态
B. 达到化学平衡状态时,反应放出的总热量可能为akJ
C. 当X、Y、Z的浓度之比为1:2:3时,反应达到化学平衡状态
D. 降低反应温度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图提供的信息,下列所得结论不正确的是( )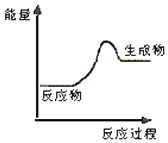
A.该反应可能为吸热反应
B.该反应一定有能量转化成了生成物的化学能
C.反应物比生成物稳定
D.生成物的总能量高于反应物的总能量,反应不需要加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )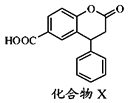
A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1mol化合物X最多能与7molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程能使蛋白质变性的是( )
A.蛋白质中加Na2SO4后析出蛋白质
B.蛋白质用福尔马林浸泡
C.蛋白质中加Pb(Ac)2后析出蛋白质固体
D.蛋白质中遇X光后
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收利用废旧锂离子电池正极材料锰酸锂(LiMn2O4)的一种流程如下:
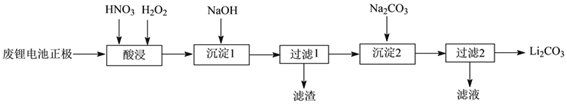
(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是_________。
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为Mn(NO3)2、LiNO3等产物。请写出该反应离子方程式_________。
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是_________。
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是_________。
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成LiMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是________。
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH]:向Mn(OH)2中边搅拌边加入_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸乙酯,如图1所示实验装置: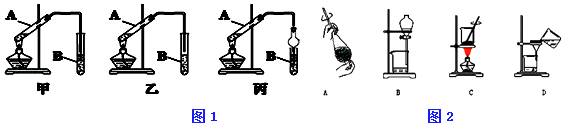
请回答下列问题:
(1)能完成本实验的装置是(从甲、乙、丙中选填)
(2)试管B中装入的液体为 . 试管B中发生反应的化学方程式为 .
(3)制取乙酸乙酯时加入试剂顺序为 , 发生反应的化学方程式为 .
(4)从制备乙酸乙酯所得的混合物中分离、提纯乙酸乙酯时,需要经过多步操作,下列图2示的操作中,肯定需要的化学操作是(选填答案编号).
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器.使用分液漏斗前必须;某同学在进行分液操作时,若发现液体流不下来,应采取的措施是 .
(6)用30g乙酸和40g乙醇反应,可以得到37.4g乙酸乙酯,则该实验的产率(产率指的是某种生成物的实际产量与理论产量的比值)是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 A 质子数 B 中子数 C 核外电子数 D 最外层电子数 E 电子层数 填写下列空白:
(1)原子种类由_______决定;
(2)元素种类由_______决定;
(3)元素的化学性质主要由_______决定;
(4)元素的原子半径由_______决定;
(5)元素的化合价主要由_______决定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉酶能在极短时间内催化淀粉水解,但不能使麦芽糖发生水解,这体现了酶的( )
A. 高效性和多样性 B. 催化性和专一性
C. 高效性和专一性 D. 催化性和高效性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com