
| 2 |
| A、2×10-4mol?L-1 |
| B、2×10-8mol?L-1 |
| C、1.414×10-3mol?L-1 |
| D、1×10-3mol?L-1 |
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
| W |
| W |
| X |
查看答案和解析>>
科目:高中化学 来源: 题型:
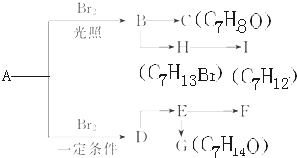
查看答案和解析>>
科目:高中化学 来源: 题型:
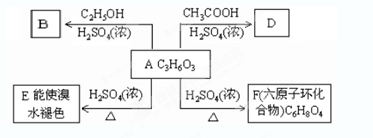
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
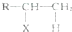 .A、B、C、D、E、M、N有下列转化关系:
.A、B、C、D、E、M、N有下列转化关系: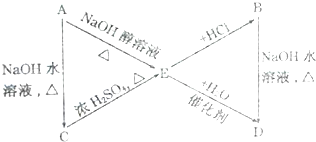
| O2 |
| 新制的Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
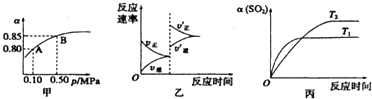
| A、由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B、点SO2、O2、SO3的平衡浓度之比为2:1:2 |
| C、达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D、压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
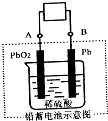 CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是2- 4 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlO2- |
| B、Al3+ |
| C、Mg2+ |
| D、Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com