
| A£® | A”¢101kPaŹ±£¬2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H=-Q kJ•mol-1£¬ŌņH2µÄČ¼ÉÕČČĪŖ$\frac{1}{2}$Q kJ•mol-1 | |
| B£® | B”¢Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2£Øg£©+Cl2£Øg£©ØT2HCl£Øg£© ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬ | |
| C£® | C”¢500”ę”¢30MPaĻĀ£¬½«0.5mol N2ŗĶ1.5mol H2ÖĆÓŚĆܱյÄČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3£Øg£©£¬·ÅČČ3kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖN2£Øg£©+3H2£Øg£© $?_{“߻ƼĮ}^{500”ę£¬30MPa}$2NH3£Øg£©”÷H=-38.6kJ•mol-1 | |
| D£® | H+£Øaq£©+OH-£Øaq£©ØTH2O£Øl£©”÷H=-57.3kJ•mol-1£¬Ōņŗ¬1mol NaOHµÄĒāŃõ»ÆÄĘČÜŅŗÓėŗ¬0.5mol H2SO4µÄÅØĮņĖį»ģŗĻŗó·Å³ö57.3kJµÄČČĮæ |
·ÖĪö A”¢Č¼ÉÕČČÖøŌŚ25”ę£¬101 kPaŹ±£¬1 molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±Ėł·Å³öµÄČČĮ棬½Š×öøĆĪļÖŹµÄČ¼ÉÕČČ£®µ„Ī»ĪŖkJ/mol£¬Éś³ÉµÄĖ®Ó¦ĪŖŅŗĢ¬£»
B”¢·“Ó¦ČČÓėĢõ¼žĪŽ¹Ų£»
C”¢0.5molN2ŗĶ1.5molH2ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3£Øg£©£¬·ÅČČ19.3kJ£¬Éś³ÉµÄ°±ĘųµÄĪļÖŹµÄĮæŠ”ÓŚ1mol£»
D”¢ÅØĮņĖįČÜÓŚĖ®·ÅČČ£¬Ōņŗ¬0.5mol H2SO4µÄÅØĮņĖįÓė1molĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦ŗó·Å³öČČĮæ“óÓŚ57.3 kJ£®
½ā“š ½ā£ŗA”¢101kPaŹ±£¬2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H=-Q kJ•mol-1£¬Éś³ÉĘųĢ¬Ė®²»ŹĒĪČ¶ØµÄ»ÆŗĻĪļ£¬ĖłŅŌH2µÄČ¼ÉÕČČ“óÓŚ$\frac{1}{2}$Q kJ•mol-1£¬¹ŹA“ķĪó£»
B”¢·“Ó¦ČČÓėĢõ¼žĪŽ¹Ų£¬ĖłŅŌĶ¬ĪĀĶ¬Ń¹ĻĀ£¬H2£Øg£©+Cl2£Øg£©ØT2HCl£Øg£© ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬£¬¹ŹBÕżČ·£»
C”¢0.5molN2ŗĶ1.5molH2ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3£Øg£©£¬·ÅČČ19.3kJ£¬Éś³ÉµÄ°±ĘųµÄĪļÖŹµÄĮæŠ”ÓŚ1mol£¬ĖłŅŌÉś³É2mol°±Ęų£¬·Å³öµÄČČĮæ“óÓŚ38.6kJ£¬¹ŹC“ķĪó£»
D”¢H+£Øaq£©+OH-£Øaq£©=H2O£Øl£©”÷H=-57.3 kJ/mol±ķŹ¾Ļ”µÄĒæĖįÓėĻ”µÄĒæ¼īČÜŅŗµÄ·“Ó¦£¬¶ųÅØĮņĖįČÜÓŚĖ®·ÅČČ£¬µ¼ÖĀ·Å³öČČĮæĘ«øߣ¬¼“ŗ¬0.5mol H2SO4µÄÅØĮņĖįÓė1molĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦ŗó·Å³öČČĮæ“óÓŚ57.3 kJ£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·½³ĢŹ½µÄÓ¦ÓĆ”¢ÖŠŗĶČČ”¢Č¼ÉÕČȵÄøÅÄīµČÖŖŹ¶£¬Ć÷Č·Č¼ÉÕČČ”¢ÖŠŗĶČȵÄøÅÄīĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕČČ»Æѧ·½³ĢŹ½µÄŹéŠ“ŌŌņ¼°±ķŹ¾ŅāŅ壬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®


 ³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż |
| ČÜŅŗ | NaCl | CH3COONH4 | NaClO | NaHCO3 | Na2CO3 |
| pH | 7.0 | 7.0 | 10.3 | 8.3 | 11.6 |
| A£® | ĖįŠŌµÄĻą¶ŌĒæČõ£ŗHClO£¼HCO3- | |
| B£® | ÓÉĖ®µēĄė²śÉśµÄc£ØH+£©£ŗ¢Ł=¢Ś | |
| C£® | ČÜŅŗ¢Ū¢ÜÖŠĖįøłĄė×ÓÅØ¶Č£ŗc£ØClO-£©£¾c£ØHCO3-£© | |
| D£® | ŌŚ¢Ü¢ŻČÜŅŗµČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØHCO3-£©+c£ØCO32-£©+c£ØH2CO3£©=0.1 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
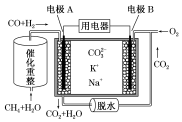
| A£® | ·“Ó¦CH4+H2O $\frac{\underline{\;“߻ƼĮ\;}}{”÷}$3H2+CO£¬ĆæĻūŗÄ1mol CH4×ŖŅĘ6NAµē×Ó | |
| B£® | µē¼«AÉĻH2²ĪÓėµÄµē¼«·“Ó¦ĪŖH2+CO32--2e-=CO2+H2O | |
| C£® | µē³Ų¹¤×÷Ź±£¬CO32-Ļņµē¼«BŅĘ¶Æ | |
| D£® | µē¼«BÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖO2+2CO2+4e-=2CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “Ö¹čµÄÖĘČ”£ŗSiO2+CØTSi+CO2”ü | |
| B£® | ³ąĢśæóÓėĻ”ŃĪĖįµÄ·“Ó¦£ŗFe3O4+8H+ØTFe2++2Fe3++4H2O | |
| C£® | ĻņBa£ØOH£©2ČÜŅŗ¼ÓČė¹żĮæNaHCO3ČÜŅŗ£ŗ2HCO3-+Ba2++2OH-ØTBaCO3”ż+2H2O+CO32- | |
| D£® | ĻņÉÕ¼īČÜŅŗÖŠĶØČėĀČĘųæÉÖĘČ”ĘÆ°×·Ū£ŗCl2+2NaOHØTNaCl+NaClO+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéŹĀŹµ | ½įĀŪ | |
| A | ½«”°84”±Ļū¶¾Ņŗ£Øŗ¬NaClO£©µĪČėĘ·ŗģČÜŅŗÖŠ£¬ĶŹÉ«»ŗĀż£¬ČōĶ¬Ź±¼ÓČėŹ³“×£¬ŗģÉ«ŗÜæģĶŹĪŖĪŽÉ« | ĖęČÜŅŗpH¼õŠ”£¬”°84”±Ļū¶¾ŅŗµÄŃõ»ÆÄÜĮ¦ŌöĒæ |
| B | ±½·ÓŗĶĖ®µÄ×ĒŅŗÖŠ£¬¼ÓĢ¼ĖįÄĘČÜŅŗ£¬ČÜŅŗ±ä³ĪĒå | ±½·ÓµÄĖįŠŌ±ČĢ¼ĖįĒæ |
| C | Ķ·ÅČėĻ”ĮņĖįÖŠ£¬ĪŽĆ÷ĻŌĻÖĻó£¬ŌŁ¼ÓČėĻõĖįÄĘ¹ĢĢ壬ČÜŅŗ±äĄ¶£¬ÓŠĆ÷ĻŌµÄĘųÅŻ·Å³ö£¬ĶČܽā | ĻõĖįÄĘæÉŅŌ¼ÓæģĶÓėĻ”ĮņĖįµÄ·“Ó¦ĖŁĀŹ |
| D | Ļņ1 mL 0.1 mol/LµÄĻõĖįŅųČÜŅŗÖŠ¼ÓČė1 mL0.1 mol/LNaClČÜŅŗ£¬³öĻÖ°×É«³Įµķ£¬ŌŁ¼ÓČė¼øµĪ0.1 mol/L NaBrČÜŅŗ£¬ÓŠµ»ĘÉ«³ĮµķÉś³É | ĀČ»ÆŅųµÄČܽā¶ČŠ”ÓŚäå»ÆŅų |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °¢·üŁ¤µĀĀŽ³£Źż¾ĶŹĒ6.02”Į1023 | |
| B£® | 1molČĪŗĪĪļÖŹ¶¼Ō¼ŗ¬ÓŠ6.02”Į1023·Ö×Ó | |
| C£® | 3.01”Į1023 øöNa+µÄĪļÖŹµÄĮæŹĒ0.5 mol | |
| D£® | 2molSO42-Ō¼ŗ¬1.204”Į1024 SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé | ĻÖĻó | ½įĀŪ |
| A | ½«¹żĮæĢś·Ū¼ÓČėĻ”ĻõĖįÖŠ£¬³ä·Ö·“Ó¦ŗóµĪ¼ÓKSCNČÜŅŗ | ÓŠĘųĢåÉś³É£¬ČÜŅŗ³ŹŃŖŗģÉ« | Ļ”ĻõĖį½«FeŃõ»ÆĪŖFe3+ |
| B | ÅØĮņĖįµĪČėÕįĢĒÖŠ£¬²¢½Į°č | µĆŗŚÉ«ÅīĖɵĹĢĢå²¢ÓŠ“Ģ¼¤ŠŌĘųĪ¶ĘųĢå | øĆ¹ż³ĢÖŠÅØĮņĖį½öĢåĻÖĪüĖ®ŠŌŗĶĶŃĖ®ŠŌ |
| C | ĻņFeCl2ČÜŅŗÖŠ¼ÓČė×ćĮæNa2O2·ŪÄ© | ³öĻÖŗģŗÖÉ«³ĮµķŗĶĪŽÉ«ĘųĢå | FeCl2ČÜŅŗ²æ·Ö±äÖŹ |
| D | Ļņ¹żĮæFeI2ČÜŅŗÖŠĻȵĪ¼Ó¼øµĪµķ·ŪČÜŅŗ£¬ŌŁµĪ¼Ó¼øµĪŠĀÖĘĀČĖ® | ČÜŅŗ±äĄ¶ | »¹ŌŠŌ£ŗI-£¾Fe2+ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com