含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m
1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:
镁铝合金
溶液
得到沉淀的质量为m
2g;
实验设计2:
镁铝合金
生成的气体在标准状况下的体积为V
1L.
实验设计3:
镁铝合金
生成的气体在标准状况下的体积为V
2L.
请回答以下问题:
(1)写出实验设计1中单质铝发生反应的离子方程式:
2Al+6H+═2Al3++3H2↑?、Al3++4OH-═[Al(OH)4]-或Al3++3OH-═Al(OH)3↓?Al(OH)3+OH-═[Al(OH)4]-?
2Al+6H+═2Al3++3H2↑?、Al3++4OH-═[Al(OH)4]-或Al3++3OH-═Al(OH)3↓?Al(OH)3+OH-═[Al(OH)4]-?
(2)写出实验设计2中反应的离子方程式:
2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
(3)判断这几种实验设计能否求出镁的质量分数,能求出的用题目提供的数据将镁的质量分数表示出来,不能求出的就空着不填.
①实验设计1
②实验设计2
③实验设计3
.










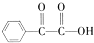


 )氧化生成,写出该反应的化学方程式:
)氧化生成,写出该反应的化学方程式:

 )经浓硫酸催化而生成,写出该反应的化学方程式:
)经浓硫酸催化而生成,写出该反应的化学方程式:


