
| A. | 探究SO2和Na2O2可能化合生成Na2SO4 | |
| B. | 探究NO和N2O可能化合生成NO2 | |
| C. | 探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3 | |
| D. | 探究红色酚酞试液通入Cl2褪色,原因是溶液酸碱性改变或被漂白 |
分析 A.二氧化硫具有较强还原性,容易被氧化,过氧化钠具有强氧化性,反应产物中可能会含有硫酸钠;
B.NO中氮元素化合价为+2价,N2O化合价是+1价,化合生成NO2时化合价都升高,不符合氧化还原反应的本质特征;
C.NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3,依据氧化还原反应的化合价变化特征分析;
D.氯气和碱反应,减小了溶液中的氢氧根离子浓度,氯气与水反应生成次氯酸具有漂白性,能够使酚酞褪色.
解答 解:A.二氧化硫具有还原性,过氧化钠具有氧化性,SO2和Na2O2反应可能有Na2SO4生成,该探究具有实际意义,故A错误;
B.NO中N元素化合价是+2价,N2O中N元素的化合价为+1价,二氧化氮中N元素的化合价为+4价,发生氧化还原反应生成NO2时化合价都升高,不符合氧化还原反应的本质特征,不必探究即可否决该猜想,所以该探究没有意义,故B正确;
C.NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3,氮元素化合价从+4价变为+5价和+3价,符合氧化还原反应的规律特征,有探究的意义,故C错误;
D.氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,消耗氢氧化钠溶液,滴有酚酞的红色溶液褪色,而氯气可以与水反应生成的次氯酸,次氯酸具有强氧化性,能够使有色物质褪色,所以该探究有意义,故D错误;
故选B.
点评 本题考查了物质性质实验方案的设计,题目难度中等,注意掌握常见物质组成及化学性质,可以依据质量守恒定律、氧化还原反应规律、物质间的反应规律等知识进行判断,试题侧重考查学生的分析、理解能力.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题
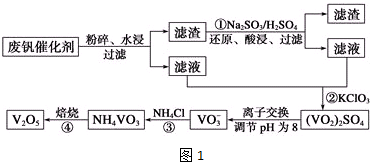
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
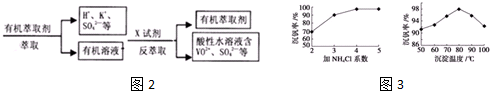
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaHCO3溶液中:K+、Cl-、AlO2-、SO42- | |
| B. | 加入铝粉能产生H2的溶液中:Na+、Fe3+、Cl-、NO3- | |
| C. | c(OH-)/c(H+)=1012的溶液中:SO32-、NO3-、K+ | |
| D. | 含有大量MnO4-的溶液中:H+、Ca2+、K+、Cl-、C2O42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

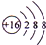 .A+、C2-、D-中离子半径最小的是Na+.
.A+、C2-、D-中离子半径最小的是Na+. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的熔沸点逐渐升高 | B. | 氢化物的稳定性逐渐增强 | ||
| C. | 单质的氧化性逐渐增强 | D. | 元素的非金属性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有③④ | C. | 只有①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气可供人呼吸但会使食物变质 | |
| B. | 化肥能促进植物生长但会污染土壤 | |
| C. | 一氧化碳可用于冶炼金属但会使人中毒 | |
| D. | 二氧化碳能灭火但会造成酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含四种元素的原子半径由小到大的顺序为:H<O<N<C | |
| B. | 同周期的三种元素的得电子能力由大到小的顺序为:O>N>C | |
| C. | 与足量烧碱溶液共热的离子方程式为:NH4++OHˉ$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com