
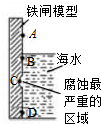
 铁及其化合物与生产、生活关系密切.
铁及其化合物与生产、生活关系密切.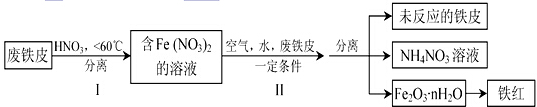
| c(CO2) |
| c(CO) |
| ||
| ||
| c(CO2) |
| c(CO) |
| 1 |
| 0.25 |
| 0.01 |
| x-0.01 |


科目:高中化学 来源: 题型:
| A、高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA | ||||
| B、室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
D、5NH4NO3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n=2x=y | ||
B、n=
| ||
| C、n=x=2y | ||
| D、x=2n=y |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
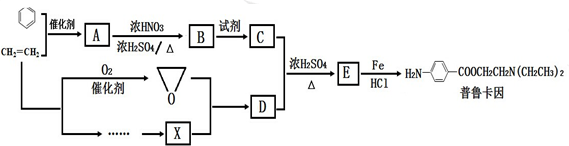
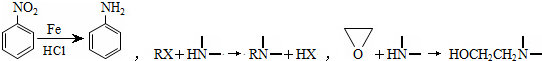
查看答案和解析>>
科目:高中化学 来源: 题型:
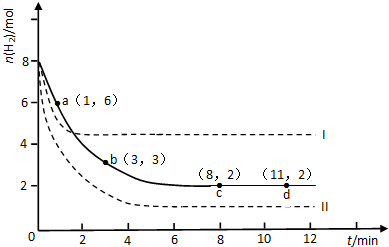
查看答案和解析>>
科目:高中化学 来源: 题型:
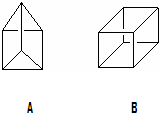 有机物A和B都是重要的化工原料,认真观察A和B的结构回答下列问题:
有机物A和B都是重要的化工原料,认真观察A和B的结构回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、四氯化碳 | B、石墨 |
| C、金刚石 | D、水晶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com