
分析 (1)根据原子守恒:n(Cu)=n[Cu(OH)2],然后根据m=nM进行计算求解;
(2)n(HNO3)=n(NaNO3)+n(NO)=n(NaOH)+$\frac{2}{3}$n(Cu),然后根据c=$\frac{n}{V}$进行计算求解.
解答 解:(1)根据铜原子守恒:n(Cu)=n[Cu(OH)2]=$\frac{29.4g}{98g/mol}$=0.3mol,所以m(Cu)=0.3mol×64g/mol=19.2g,
答:反应消耗铜的质量为19.2g;
(2)n(HNO3)=n(NaNO3)+n(NO)=n(NaOH)+$\frac{2}{3}$n(Cu)=1L×1mol/L+$\frac{2}{3}$×0.3mol=1.2mol,所以c=$\frac{n}{V}$=$\frac{1.2mol}{0.5L}$=2.4mol/L,
答:稀硝酸的物质的量浓度为2.4mol/L.
点评 本题考查铜与硝酸发生氧化还原反应的计算,题目难度较大,明确反应过程、充分利用守恒计算是解题的关键,试题培养了学生的分析、理解能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1molgL-1的溶液:Na+、K+、SiO32-、NO3- | |
| B. | 加苯酚显紫色的溶液:K+、NH4+、Cl-、I- | |
| C. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- | |
| D. | 通足量SO2后的溶液:Na+、NH4+、ClO-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
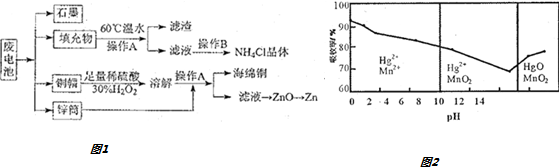
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,立即用水扑灭 | |
| B. | 稀释浓硫酸时,将水倒入浓硫酸中 | |
| C. | 在量筒中配置100mL,1mol/L NaCl溶液 | |
| D. | 大量氯气泄漏时,尽量沿高处迅速离开现场 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
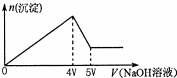 向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )| A. | 1:2 | B. | 1:1 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先滴加氯水,再滴加KSCN溶液后显红色 | |
| B. | 先滴加KSCN溶液,不显红色,再滴加氯水后显红色 | |
| C. | 滴加NaOH溶液,产生红褐色沉淀 | |
| D. | 滴加KSCN溶液,溶液呈红色,再加足量铁粉红色消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和滴定时盛待测的锥形瓶中有少量水对滴定结果无影响 | |
| B. | 在酸碱中和滴定实验中,滴定管都需要润洗,否则引起误差 | |
| C. | 滴定时,左手控制滴定管的活塞,右手握持锥形瓶,边滴加振荡,眼睛注视滴定管中的液面 | |
| D. | 在酸碱中和滴定实验中,滴定前仰视滴定后俯视会引起误差 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体摩尔体积Vm=22.4L/mol,则气体所处的状态为标准状况 | |
| B. | 一定条件下,1.4gN2和0.2molH2混合充分反应,转移的电子数目约为1.806×1023个 | |
| C. | 1.0mol/L的Na3PO4溶液中含有的阴离子总数大于6.02×1022个 | |
| D. | 5.0g乙烷中含有的极性键的数目约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
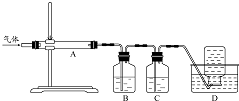 氧化镁在医药、建筑等行业应用广泛,木炭还原硫酸镁煅烧制备高纯氧化镁是一种新的探索.煅烧过程存在以下反应:
氧化镁在医药、建筑等行业应用广泛,木炭还原硫酸镁煅烧制备高纯氧化镁是一种新的探索.煅烧过程存在以下反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com