
下列说法正确的是 ( )
A.含有离子键的化合物必是离子化合物
B.含有共价键的化合物就是共价化合物
C.共价化合物可能含离子键
D.离子化合物中一定含有共价键
科目:高中化学 来源: 题型:
某反应进行过程中,各物质物质的量的变化情况如图所示。下列说法正确的是 ( )
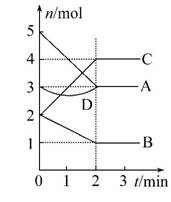
A.C、D是生成物
B.反应的方程式为2A+B====2C
C.2 min后各物质的量不再变化
D.该反应不是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知反应A+3B 2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
mol·L-1·min-1,以C的浓度变化表示的反应速率为 mol·L-1·min-1。
(2)在恒温恒容条件下,反应2SO2+O2 2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
(3)将物质的量相等的A、B混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
C的平均反应速率是0.1 mol·L-1·min-1。回答下列问题:
①x值是 。
②用B表示的5 min内的平均反应速率为_______________________________。
③反应开始前放入容器中的A、B物质的量各为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.离子键就是阴、阳离子间的静电引力
B.所有金属元素与所有非金属元素间都能形成离子键
C.NH4Cl属于离子化合物
D.在离子化合物CaCl2中,两个氯离子间也存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
为清理高速公路上的积雪使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图为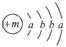 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m= ,该融雪剂的化学式为 。
(2)Z、W元素的名称为 、 。
(3)下列说法正确的是 。
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是 。
A.XY2的电子式:X2+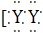 ]2-
]2-
B.WZ2的结构式:Z W
W Z
Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为Y2+Z2- 2Y-+Z↓
2Y-+Z↓
D.用电子式表示XY2的形成过程为
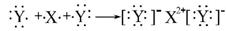
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机化合物的说法正确的是 ( )
A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别
B.戊烷(C5H12)有两种同分异构体
C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键
D.糖类、油脂和蛋白质均可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A的分子式为C8H8O2,其核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图。关于A的下列说法中,正确的是( )

A.A不能发生水解反应
B.1 mol A在一定条件下可与4 mol H2发生加成反应
C.符合题中A分子结构特征的有机物只有1种
D.A属于醚类
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室里可用如图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
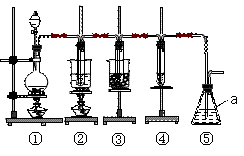
上图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里盛有紫色石蕊溶液。
请回答下列问题:
(1)仪器a的名称是_________________。
(2)实验室制取氯气的离子方程式为___________________________________________。
为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____(填字母代号)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
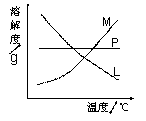 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异
是______________________________________。反应完毕
经冷却后,②的试管中有大量晶体析出。在右图中符合该晶
体溶解度曲线的是_____(填字母代号);从②的试管中分离出
晶体的操作是________,该操作需要用到的玻璃仪器有____________________________。
(4)次氯酸钠中存在的化学键类型为_______________________________。
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请完成下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为_________色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | _________________________________________ |
| 然后溶液从无色逐渐变为_________色 | _________________________________________ |
(6)装置⑤的作用是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com