
���� ��1������̿������������Ӧ�������������У���CO����CO2����CO2��CO�Ļ�������������
���ݷ�Ӧ����������������غ���д��Ӧ�����ӷ���ʽ��
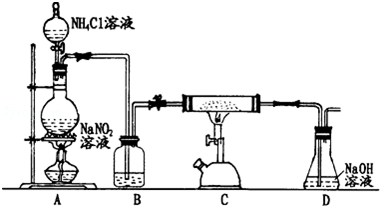
N���ٸ�ʵ���Ƕ�̼������������ͬ�����ڸ����·�Ӧ�����������е�ʵ��̽����������ʵ��װ����������ø��ݴ���ѹǿԭ��������װ�õ������ԣ�
�ۼ���ȼ�չ�ǰ����ͨһ��ʱ��N2���ž�װ���ڿ�����������ž���������ô�����е���������̿�۷�ӦӰ�췴Ӧ�������������ɣ�Bװ�õ������Ǹ���N2��
�ݸ��������غ��ж��������ɣ�
V��CO�ж�����ɢ�������л���Ⱦ��������Dװ�õ��ܴ��þƾ��Ƶ�ȼ���������ϴ��ռ���
��� �⣺��1������̿������������Ӧ�������������У���CO����CO2����CO2��CO�Ļ���
�ʴ�Ϊ��CO2��CO�Ļ���
���Ȼ�隣�����Һ���������ƣ�NaNO2��������Һ��ϼ��ȷ�Ӧ�Ƶõ�������Ӧ����NH4Cl��NaNO2��������ΪN2�����������غ㻹Ӧ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��NH4++NO2-$\frac{\underline{\;\;��\;\;}}{\;}$N2��+2H2O��
�ʴ�Ϊ��NH4++NO2-$\frac{\underline{\;\;��\;\;}}{\;}$N2��+2H2O��
N���ٸ�ʵ���Ƕ�̼������������ͬ�����ڸ����·�Ӧ�����������е�ʵ��̽����������ʵ��װ����������ã��������Ӻ�װ�ú�Ҫ����װ�õ������ԣ����Ը�����ѹԭ�������飬�رշ�Һ©���ϵĻ�����������ƿ���۲�D�ܿڣ����������ݳ���ֹͣ���Ⱥ���������ƿ����Һ��һ��ʱ����Һ���ֲ��䣬˵��װ�õ����������ã�
�ʴ�Ϊ�����װ�������ԣ�
��������ž���������ô�����е���������̿�۷�ӦӰ�췴Ӧ�������������ɣ������������ȶ��ĵ����ſ�����Bװ�õ������Ǹ���N2��
�ʴ�Ϊ���ž�װ���ڿ���������N2��
��1.60g�����������ʵ���Ϊ$\frac{1.6g}{160g/mol}$=0.01mol��
����ʯ��ˮ����ǣ�˵����CO2�������ɣ�m��C��=0.24g����n��C��=n��CO2��=$\frac{0.24g}{12g/mol}$=0.02mol����ȫ�����ɶ�����̼����m��CO2��=0.02mol��44g/mol=0.88g��ȷ����ȼ�չ��е�ʣ���������Ϊ1.12g����Ӧ��Ӳ�ʲ����ܺ����������仯Ϊ��1.6g-1.12g=0.48g����0.48g��0.88g��������������ΪCO2��CO�Ļ���
�ʴ�Ϊ��3��
V��CO�ж�����ɢ�������л���Ⱦ�������ӻ��������ĽǶȿ��ǣ�ʵ������Ҫ�Ľ��Ĵ�ʩ�ǣ���Dװ�õ��ܴ���һ����ȼ�ľƾ��ƣ���һ����̼ת���ɶ�����̼��������Dװ�õ��ܴ������ϴ��ռ�β�������Ϊ����
�ʴ�Ϊ����Dװ�õ��ܴ��þƾ��Ƶ�ȼ���������ϴ��ռ���
���� ���⿼�����̿������������Ӧ����������ijɷֵ�̽����ע��������غ�ĽǶȷ�������ǿ�����ݵĴ����ͷ�����������ֿ���ѧ���ķ�����������ѧʵ����������Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�۲���Ҫ�ܷⱣ�� | |
| B�� | FeCl2��Һ����ʱ������������ | |
| C�� | þ��Ӧ������ú���� | |
| D�� | NaOH��ҺӦ���������в��������Լ�ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | F | B�� | Cl | C�� | Br | D�� | I |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 13g �� ��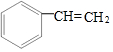 �Ļ�����к��еĵ�����Ϊ7NA �Ļ�����к��еĵ�����Ϊ7NA | |
| B�� | 60gSiO2�к��еĹ��ۼ���ĿΪ4NA | |
| C�� | ��״���£�11.2LH2��Cl2��Ӧ��õ��������к��е�ԭ������ΪNA | |
| D�� | 1molNaCO3����ˮ��������Һ��CO32-��HCO3-������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ľṹʽ��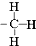 | B�� | �������Ľṹ��ʽ��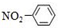 | ||
| C�� | ������ķ���ʽ��C2H5Cl | D�� | ������ӵ����ģ��ʾ��ͼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ǧ | B�� | Ǧ�Ͻ� | C�� | ʯī | D�� | ľ̿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��CH3COOH | ��H2CO3 | ��H2S | ��H3PO4 |
| K=1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=9.1��10-8 K2=1.1��10-12 | K1=7.5��10-3 K2=6.2��10-8 K3=2.2��10-13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu����ϡHNO3��Cu+2H++NO3-�TCu2++NO2��+H2O | |
| B�� | ��ʯī�缫��ⱥ��ʳ��ˮ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2�� | |
| C�� | ��NH4��2Fe��SO4��2��Һ�����NaOH��Һ��Ӧ��Fe��OH��2��Fe2++2OH-�TFe��OH��2�� | |
| D�� | ��Fe��NO3��3��Һ�м��������HI��Һ��2Fe3++2I-�T2Fe2++I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 5�� | C�� | 6�� | D�� | 7 �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com