
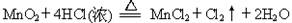


 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O CuSO4+2H2O+SO2 ↑硫酸有一半被还原所以硫酸总物质的量为2×0.9="1.8(mol)"
CuSO4+2H2O+SO2 ↑硫酸有一半被还原所以硫酸总物质的量为2×0.9="1.8(mol)" 

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题

| A.第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C.第②步中,还原0.1 mol Cr2O72-需要45.6 g FeSO4 |
| D.第③步沉淀剂a可以使用NaOH等碱性物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学方程式中产物分子的化学计量数由小到大的顺序是SO2、N2、NH3、H2O |
| B.氧化产物和还原产物的物质的量之比为3∶1 |
| C.被氧化元素原子和被还原元素原子的物质的量之比为2∶3 |
| D.若反应生成1 mol H2O,则转移的电子为6 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原混合物中铜和铁各0.15 mol |
| B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 |
| D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe3O4+S4O62-+2H2O,有关说法正确的是
Fe3O4+S4O62-+2H2O,有关说法正确的是| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x = 2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应后溶液中无硝酸亚铁 |
B.反应前HNO3溶液的浓度为2.0mol |
C.反应后溶液中c(NO3-)=1.6mol |
| D.反应后的溶液最多还能溶解1.6lgFe |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2H2↑+O2↑,下列有关判断正确的是
2H2↑+O2↑,下列有关判断正确的是| A.氧化剂是氢元素 |
| B.还原产物是O2 |
| C.H2O既有氧化性也有还原性 |
| D.2molH2O反应,转移了8mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com