
依照“同温、同压、同体积的任何气体所含分子数相同”,下列叙述正确的是( )
A.同温、同压下两种气体的体积之比等于摩尔质量之比
B.同温、同压下两种气体的物质的量之比等于密度之比
C.同温、同压下两种气体的质量之比等于密度之反比
D.同温、同体积下两种气体的物质的量之比等于压强之比
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:2017届福建省四地六校高三上第一次月考化学试卷(解析版) 题型:实验题
某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g;②称量装有试样的坩埚质量为B g;③加热;④冷却;⑤称量坩埚和残余物的质量为C g;⑥重复③至⑤操作,直至恒重,质量为D g。
(1)坩埚中发生反应的化学方程式 。
(2)计算Na2CO3质量分数必须用到的测定数据为 。
乙方案:
在天平上准确称取 0.3000g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000mol·L-1的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3,即HCl+Na2CO3 == NaHCO3+NaCl。重复上述操作两次。
(3)配制上述盐酸标准溶液100ml,若用2.0mol/LHCl进行配制,需用量筒量取该HCl溶液 ml;定容时俯视刻度线,将导致配制的溶液浓度 。(填“偏高”、“偏低”或“没有影响”)
(4)根据下表数据,样品中w(Na2CO3)= 。(用百分数表示,保留一位小数)
滴定次数 | 样品的质量/g | 稀盐酸的体积/mL | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 0.3000 | 1.02 | 21.03 |
2 | 0.3000 | 2.00 | 21.99 |
3 | 0.3000 | 0.20 | 20.20 |
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
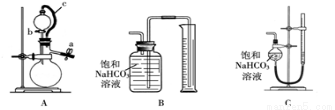
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若分液漏斗中的水无法持续滴下,试判断装置A是否漏气? (填“漏气”、“不漏气”或“无法确定”)。实验时,装置A中c的作用 , 。
(6)为了提高测定的准确性,应选用装置A和 (填写字母标号)进行实验。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
下列生产或实验事实得出的相应结论不正确的是
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | A、B两支试管,各加入4mL0.01mol/L的KMnO4酸性溶液,在A试管中加入2mL0.01mol/LH2C2O4溶液和在B试管中加入4mL 0.02mol/L的H2C2O4溶液,记录溶液褪色所需时间,B试管褪色时间短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
已知下列反应的平衡常数:H2(g)+S(s)  H2S(g) K1
H2S(g) K1
S(s)+O2 (g)  SO2(g) K2
SO2(g) K2
则反应H2(g)+ SO2(g)  O2(g)+ H2S(g)的平衡常数是
O2(g)+ H2S(g)的平衡常数是
A.K1+K2 B.K1-K2 C.K1×K2 D.K1/K2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上第一次大考化学卷(解析版) 题型:实验题
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋植物中提取碘的流程如下:

某化学兴趣小组将上述流程②③设计成如图所示:


已知氯水中含有Cl2,②中发生反应的化学方程式为Cl2+2KI=2KCl+I2。
回答下列问题:
(1)写出提取过程①③中实验操作的名称:①________________,③________________。
(2)F中的现象是________________________。
(3)从碘的四氯化碳溶液中得到单质碘还需进行的操作是________。实验装置如右图所示,该实验采用的加热方式为_____________,仪器A的名称为__________________。

(4)在灼烧过程中,将使用到的(除泥三角外)实验仪器有____________。
A试管 B瓷坩埚 C坩埚钳 D蒸发皿 E酒精灯
(5)现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL CCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏 斗活塞和上口的玻璃塞是否漏液;
斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
完成下列填空:
①正确操作步骤的顺序是:(用上述各操作的编号字母填写)
 → → →A→_________→G→E→F
→ → →A→_________→G→E→F
②上述G步骤操作的目的是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上第一次大考化学卷(解析版) 题型:选择题
下列离子检验的方法正确的是( )
A.向某溶液中加入少量硝酸银溶液,生成白色沉淀,说明原溶液中有Cl-
B.向某溶液中加入少量氯化钡溶液,生成白色沉淀,说明原溶液中有SO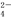
C.向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,说明原溶液中有CO32-
D.向某溶液中加入足量盐酸,无现象,再加入少量BaCl2溶液,产生白色沉淀,说明原溶液中有SO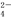
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上第一次大考化学卷(解析版) 题型:填空题
在一定温度下,有A.盐酸 B.硫酸 C.醋酸 三种酸:(用a、b、c表示)
(1) 当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是_____________。
(2) 同体积、同物质的量浓度的三种酸,消耗NaOH的量由大到小的顺序是____________。
(3) 若三者c(H+)相同时,物质的量浓度由大到小的顺序是_____________。
(4) 当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是___________。
(5) 将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上开学考试化学试卷(解析版) 题型:填空题
同温、同压时质量相等的O2和O3相比较,其物质的量之比为____________,体积之比为___________ 密度之比为_____________,所含氧原子数之比为______________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上第一次月考化学卷(解析版) 题型:填空题
现有m g某气体,它由四原子分子构成,它的摩尔质量为M g·mol-1,则:
(1)该气体的物质的量为 mol.
(2)该气体中所含的原子总数为 个.
(3)该气体在标准状况下的体积为 L.
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为 .
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为 mol·L-1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com