
液态氨中可电离出极少量的NH2-和NH4+。下列说法正确的是
A.NH3属于离子化合物 B.常温下,液氨的电离平衡常数为10-14
C.液态氨与氨水的组成相同 D.液氨中的微粒含相同的电子数
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查(二)化学试卷(解析版) 题型:填空题
(14分)X、Y、Z、M四种短周期元素的原子半径依次减小。甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3;乙是日常生活的基础能源,其中含元素Y的质量分数为75%;丙是具有强氧化性的弱酸。丁为丙的钠盐,常用于漂白或消毒。戊与甲的组成元素相同,其分子具有18电子。请按要求回答下列问题:
(1)元素X、Y的最高价氧化物的水化物的酸性由强到弱为(填化学式)_______;丁的电子式为___________;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)______________、______________。
(2)元素E、F与X同周期。
①常温下E的单质与甲反应缓慢,加热至沸反应迅速,滴加酚酞试液,溶液变红色;此反应的化学方程式为 。
②F的单质粉末加油漆后即得“银粉漆”,在汽车漆家族中有重要地位。写出保存“银粉”时的注意事项:________________、__________________等。
(3)向盛有一定浓度戊溶液的烧杯中逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中可依次观察到的现象:
a.浅绿色溶液变成黄色
b.有少量气泡产生,片刻后反应变得更剧烈,并放出较多热量
c.继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀
①现象a中反应的离子方程式:________________________________________;
②现象b中反应剧烈的化学方程式:____________________________________;
③解释现象c:________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市第二次诊断性测试化学试卷(解析版) 题型:实验题
(16分)硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于滴定实验某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质
已知:Na2SO3 + S = Na2S2O3
I.制备 Na2S2O3
(1)如图,组装好仪器,检验完气密性(气密性良好),各装置试剂均装入后的下一步操作是______
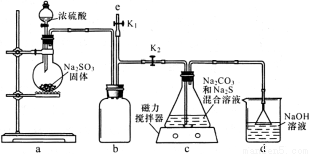
(2)反应开始后,C中发生了多个化学反应写出其中任意一个非氧化还原反应的方程式_____________
(3)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1 ,其目的是______待c中溶液冷却后,倒入蒸发皿,通过加热蒸发冷却结晶和干燥等操作获得Na2S2O3·5H2O晶体
Ⅱ.探究Na2S2O3的部分化学性质
【提出假设】
假设一:Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3 溶液pH=7
假设二:从S元素的化合价推测Na2S2O3具有较强的还原性
【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空)
实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
假设一 | ___________________ | 溶液pH=8 | ________________________ |
假设二 | 向溴水中滴入适量Na2S2O3溶液 | 溴水褪色 | ___________________________ |
【实验结论】__________________
Ⅲ:用Na2S2O3的溶液测定溶液中ClO2的物质的量浓度,可进行以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL(已知:I2+2S2O32-=2I-+S4O62-)
根据上述步骤计算出原ClO2溶液的物质的量浓度为 mol·L-1(用含字母的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
25℃时,NH3· H2O和CH3COOH的电离常数K相等。下列说法正确的是
A.常温下,CH3COONH4溶液的pH=7,与纯水中H2O的电离程度相同
B.向CH3COONH4溶液加入CH3COONa固体时,c(NH4+)、c(CH3COO-)均会增大
C.常温下,等浓度的NH4Cl和CH3COONa两溶液的pH之和为14
D.等温等浓度的氨水和醋酸两溶液加水稀释到相同体积,溶液pH的变化值一定相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
某未知溶液可能含Na+、NH4+、Fe2+、I-、Cl-、CO32-、SO32-。将该溶液加少量新制氯水,溶液变黄色。再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象。下列推断合理的是
A.一定存在Fe2+、Na+、Cl- B.一定不存在I-、SO32-
C.一定呈碱性 D.一定存在NH4+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
结构片段为…―CH2―CH=CH―CH2―…的高分子化合物的单体是
A.乙烯 B.乙炔 C.正丁烯 D.1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
(14分)研究氮及其化合物的性质在人类进步过程中具有极为重要的意义。
(1)已知反应:
①2H2(g)+O2(g) 2H2O(g) △H=-483.6 kJ/mol
2H2O(g) △H=-483.6 kJ/mol
②N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
③4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ/mol
4NO(g)+6H2O(g) △H=-905kJ/mol
则反应④4NH3(g)+3O2(g) 2N2(g)+6H2O(g)的△H=___________。
2N2(g)+6H2O(g)的△H=___________。
(2)在恒温恒容的甲容器,恒温恒压的乙容器中分别进行合成氨反应(图中所示数据均为初始物理量)。t分钟后反应均达到平衡,生成NH3均为0.4mol(忽略水对压强的影响及氨气的溶解)。
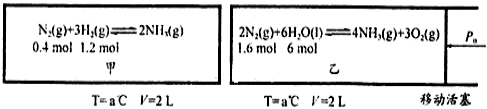
①该条件下甲容器中反应的平衡常数K= ;平衡时,甲容器的压强P = (初始压强用P0表示)。
②该条件下,若向乙中继续加入0.2 mol N2,达到平衡时N2转化率= 。
(3)在实验室中,某同学利用下列试剂及器材完成的实验能够证明NH3·H2O是弱电解质的是_________(选填字母代号)。
A.用氨水做导电性实验,灯泡昏暗
B.将氨水滴入AlCl3溶液中,产生白色沉淀
C.常温下,用pH试纸测得0.1mol/L氨水的pH<13
D.用湿润的蓝色石蕊试纸测得NH4Cl溶液为紫色
(4)常温下,向1molL-1NH4Cl溶液中通入少量的NH3此时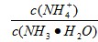 的值 (填“增大”、“减小”或“不变”);若将1molL-1NH4Cl溶液和1molL-1NaOH溶液混合后溶液恰好呈中性,则混合前NH4Cl溶液的体积 NaOH溶液的体积(填“大于”、“小于”或“等于”).
的值 (填“增大”、“减小”或“不变”);若将1molL-1NH4Cl溶液和1molL-1NaOH溶液混合后溶液恰好呈中性,则混合前NH4Cl溶液的体积 NaOH溶液的体积(填“大于”、“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
[Fe(CN)6]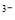 可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]
可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]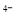 。工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理。下列说法不正确的是
。工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理。下列说法不正确的是
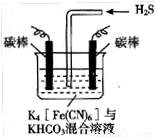
A.电解时阳极反应式为[Fe(CN)6]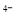 -e
-e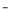
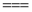 [Fe(CN)6]
[Fe(CN)6]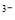
B.电解时阴极反应式为+2 e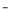
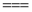 H2
H2 +2CO
+2CO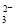
C.当电解过程中有22.4L标准状况下的H2生成时,溶液中有32gS析出(溶解忽略不计)
D.整个过程中需要不断补充K4 [Fe(CN)6]与KHCO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
下列物质能用于制造光导纤维的是
A.钢 B.陶瓷 C.聚乙烯 D.二氧化硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com