
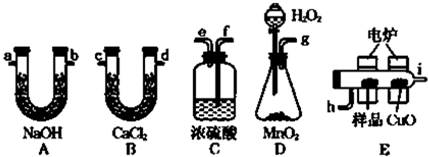
| m |
| M |
| 2.16g |
| 18g/mol |
| 9.24g |
| 44g/mol |
| 0.48g |
| 16g/mol |
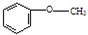 ,
, .
.


科目:高中化学 来源: 题型:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | … | 29 |
| C2H6 | C2H6O | C2H4O2 | C3H8 | C3H8O | C3H6O2 | C4H10 | … | X |
| A、X的分子式为C11H24O |
| B、X可能与金属钠反应生成氢气 |
| C、X可能与碳酸钠反应放出CO2气体 |
| D、X可能与第30项发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B、铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| C、绿色化学的核心是从源头上消除工业生产对环境的污染 |
| D、用CO2合成聚碳酸酯可降解塑料,可实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 高温高压 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
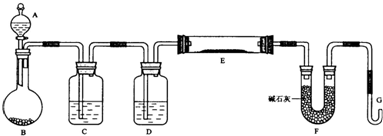
查看答案和解析>>
科目:高中化学 来源: 题型:
| 一定条件 |
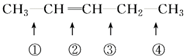 发生此反应时断裂的化学键应是( )
发生此反应时断裂的化学键应是( )| A、①④ | B、①③ | C、② | D、②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com