
| 放电 |
| 充电 |
| A、电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 |
| B、电池放电后,电池中溶液的pH变大 |
| C、电池充电时,阴极反应为:PbSO4(s)+2H2O(l)-2e-═PbO2(s)+4H+(aq)+SO42-(aq) |
| D、电池充电时,把铅蓄电池的正极与外电源负极相连 |
| 放电 |
| 充电 |


科目:高中化学 来源: 题型:
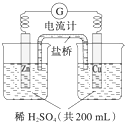 (1)原电池的负极反应式是
(1)原电池的负极反应式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | |
| C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(Zn)=6.5g?min-1 |
| B、v(H2SO4)=0.05mol?L-1?min-1 |
| C、v(SO42-)=0.02mol?L-1?min-1 |
| D、v(H2)=22.4mL?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
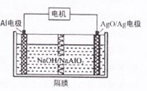 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示,下列有关说法错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示,下列有关说法错误的是( )| A、电池反应为:2Al+3AgO+2NaOH═2NaAlO2+3Ag+H2O |
| B、当电极上析出1.08gAg时,电路中转移的电子为0.02mol |
| C、电子流动方向为:Al电极→电机→AgO/Ag电极→Al电极 |
| D、负极反应为Al-3e+4OH=AlO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热的化学反应都是吸热反应 |
| B、中和反应都是放热反应 |
| C、原电池是将电能转化为化学能的一种装置 |
| D、只要有能量变化的都是化学变化、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①比②多 | B、①比②少 |
| C、一样多 | D、无法比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com