
【题目】设NA为阿伏伽德罗常数,下面叙述正确的是( )
A.标准状况下,11.2L CCl4所含分子数为0.5NA
B.1L 1mol/L的氯化钠溶液中,所含离子数为NA
C.常温下,4.4g CO2和N2O(不反应)混合物中所含有的原子数为0.3NA
D.1mol Cl2与足量的铁发生反应,转移的电子总数为3NA
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】(多选)氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42﹣、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1: 
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
A.沉淀1的主要成分为Al(OH)3和Fe(OH)3
B.溶液2中所含金属阳离子只有Mg2+
C.将溶液3蒸干即得CuSO45H2O晶体
D.若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2是一种食品添加剂,它与酸性KMnO4溶液发生反应 MnO4﹣+NO2﹣+X→Mn2++NO3﹣+H2O(未配平).下列叙述中正确的是( )
A.生成1 mol NaNO3需消耗0.4 mol KMnO4
B.反应过程中溶液的pH减小
C.该反应中NO ![]() 被还原
被还原
D.X可以是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.
(1)Ti基态原子的电子排布式为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物.电负性:C(填“>”或“<”,下同)B;第一电离能:NO,原因是 .
(3)月球岩石﹣﹣玄武岩的主要成分为钛酸亚铁(FeTiO3).FeTiO3与80%的硫酸反应可生成TiOSO4 . SO42﹣的空间构型为形,其中硫原子采用杂化,写出SO42﹣的一种等电子体的化学式:
(4)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3 , CaTiO3的晶体结构如图所示(Ti4+位于立方体的顶点).该晶体中,Ti4+和周围个O2﹣相紧邻. 
(5)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型.晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响.由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71gcm﹣3 , 晶胞边长为4.28×10﹣10 m,则FexO中x=(用代数式表示,不要求算出具体结果).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是重要的有机化合物,可由E和F在一定条件下合成:(有些反应条件省略,如加热等) 
已知以下信息:
①A属于芳香烃,H属于酯类化合物;②I的核磁共振氢谱为二组峰,且峰的面积比为6:1.
回答下列问题:
(1)B的结构简式 , D的官能团名称 .
(2)B→C的反应类型; D→E的反应类型 ,
(3)①C→D的化学方程式 . ②E+F→H的化学方程式 .
③I→G的化学方程式 .
④G→J的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.所有不锈钢都只含有金属元素
B.我国流通的硬币材质是金属单质
C.广东打捞的明代沉船上存在大量铝制餐具
D.镁合金的硬度和强度均高于纯镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝硅合金(含硅15.5%)在凝固时收缩率很小,因而这种合金适合铸造,现有下列3种晶体:①铝②硅③铝、硅合金,它们的熔点从低到高的顺序是( )
A.①②③
B.②①③
C.③②①
D.③①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H(布洛芬)是临床常用的镇痛消炎药,其合成路线如下(部分反应条件和试剂略): 
已知:(1) ![]() (R1、R2代表烷基);(2)
(R1、R2代表烷基);(2) ![]() +ClCH2COOR4+R4ONa→
+ClCH2COOR4+R4ONa→ ![]() COOR4+R4OH+NaCl(R3、R4代表烷基)
COOR4+R4OH+NaCl(R3、R4代表烷基)
请回答下列问题:
(1)化合物H的分子式是 , 化合物B的官能团名称是 , 第③步的化学反应类型是
(2)第②步反应的化学方程式是 .
(3)化合物G的结构简式是 .
(4)第④步反应的化学方程式是 .
(5)同时满足下列条件的H的所有同分异构体的结构简式是 .
I.结构中有苯环,无﹣O﹣O﹣;II.核磁共振氢谱为4组峰,峰面积之比为2:2:1:1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( ) 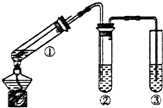
A.上下移动①中铜丝可控制生成SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.该反应中浓硫酸表现了强氧化性和脱水性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com