
| A. | 22 | B. | 24 | C. | 20 | D. | 25 |
分析 反应①的平衡常数k=c(NH3)•c(HI),NH4I分解生成的HI为平衡时HI与分解的HI之和,即为NH4I分解生成的NH3,由反应②可知分解的c(HI)为平衡时c(H2)的2倍,求出为NH4I分解生成的NH3,代入反应①的平衡常数k=c(NH3)•c(HI)计算.
解答 解:平衡时c(HI)=4mol•L-1,HI分解生成的H2的浓度为1mol•L-1.
NH4I分解生成的HI的浓度为4mol•L-1+2×1mol•L-1=6mol•L-1,所以NH4I分解生成的NH3的浓度为6mol•L-1,
所以反应①的平衡常数k=c(NH3)•c(HI)=6mol•L-1×4mol•L-1=24mol2•L-2.
故选B.
点评 本题的解题关键在于平衡时HI为NH4I分解生成的HI与分解的HI之差,注意两个平衡的关系,题目难度中等.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:解答题
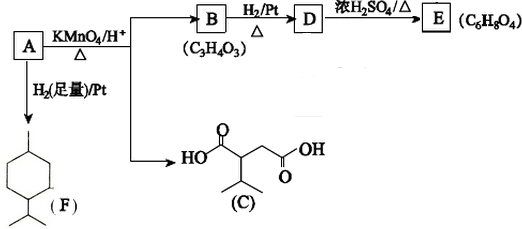
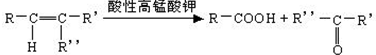
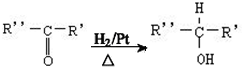
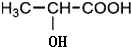 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$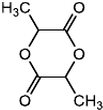 +2H2O.
+2H2O. ,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).
,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
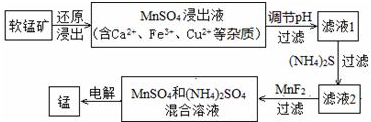
| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol/(L•s) | B. | v(B)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=0.4 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42- | |
| B. | PH=1的溶液中:K+、Fe2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ | |
| C. | 新鲜的空气中:SO2、NO、N2、NH3 | |
| D. | 所有氯气的集气瓶中:H2S、H2、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法确定 | B. | a<b | C. | a=b | D. | a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入烧碱 | B. | 加入盐酸 | C. | 升高温度 | D. | 加水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com