
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
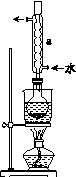
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s)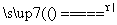 Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O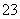 +I2===S4O
+I2===S4O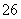 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
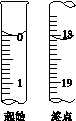
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
(1)使硫粉易于分散到溶液中
(2)冷凝管 冷凝回流
(3)Na2SO4 取少量产品溶于过量盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4
(4)S2O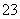 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O
(5)由无色变蓝色
(6)18.10  ×100%
×100%
(7)S2O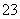 +4Cl2+5H2O===2SO
+4Cl2+5H2O===2SO +8Cl-+10H+
+8Cl-+10H+
[解析] (1)硫粉难溶于水,微溶于乙醇,故硫粉用乙醇润湿后易扩散到溶液中。(2)装置中仪器a是冷凝管,起冷凝回流汽化的反应物的作用。(3)因反应物Na2SO3易被空气中的氧气氧化成Na2SO4,故可能存在的无机杂质是Na2SO4;检验产品中是否含有Na2SO4,即检验SO 是否存在,需要防止SO
是否存在,需要防止SO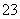 的干扰,故不能用具有强氧化性的硝酸酸化,而应用盐酸酸化,过滤除去不溶物,再向滤液中滴加氯化钡溶液。(4)产品发黄,说明产品中含有硫杂质,这是由于在酸性环境中Na2S2O3不稳定,发生歧化反应:2H++S2O
的干扰,故不能用具有强氧化性的硝酸酸化,而应用盐酸酸化,过滤除去不溶物,再向滤液中滴加氯化钡溶液。(4)产品发黄,说明产品中含有硫杂质,这是由于在酸性环境中Na2S2O3不稳定,发生歧化反应:2H++S2O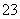 ===S↓+SO2↑+H2O所致。(5)滴定终点时,过量的单质碘使无色的淀粉溶液变蓝,可指示滴定终点。(6)起始读数为0.00 mL,终点读数为18.10 mL,所以消耗碘的标准溶液的体积为18.10 mL-0.00 mL=18.10 mL;根据2Na2S2O3·5H2O~2S2O
===S↓+SO2↑+H2O所致。(5)滴定终点时,过量的单质碘使无色的淀粉溶液变蓝,可指示滴定终点。(6)起始读数为0.00 mL,终点读数为18.10 mL,所以消耗碘的标准溶液的体积为18.10 mL-0.00 mL=18.10 mL;根据2Na2S2O3·5H2O~2S2O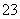 ~I2,得n(Na2S2O3·5H2O) =2n(I2)=2×0.100 0 mol·L-1×18.10×10-3 L=3.620×10-3 mol,则产品的纯度
~I2,得n(Na2S2O3·5H2O) =2n(I2)=2×0.100 0 mol·L-1×18.10×10-3 L=3.620×10-3 mol,则产品的纯度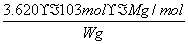 ×100%=
×100%= ×100%。(7)S2O
×100%。(7)S2O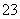 被Cl2氧化成SO
被Cl2氧化成SO ,Cl2被还原为Cl-,首先根据化合价升降总数相等写出S2O
,Cl2被还原为Cl-,首先根据化合价升降总数相等写出S2O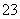 +4Cl2→2SO
+4Cl2→2SO +8Cl-,然后根据原子守恒和电荷守恒写出S2O
+8Cl-,然后根据原子守恒和电荷守恒写出S2O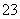 +4Cl2+5H2O===2SO
+4Cl2+5H2O===2SO +8Cl-+10OH-。
+8Cl-+10OH-。


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
[配制KMnO4标准溶液]如图是配制50 mL KMnO4标准溶液的过程示意图。
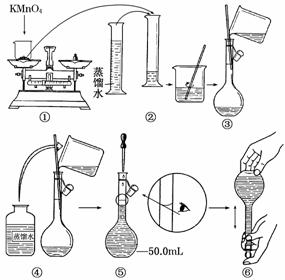
(1)请你观察图示判断,其中不正确的操作有(填序号)__________;
(2)其中确定50 mL溶液体积的容器是(填名称)__________;
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,所配制的溶液浓度将____________(填“偏大”或“偏小”)。
[测定血液样品中Ca2+的浓度] 抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)已知草酸跟KMnO4反应的离子方程式为:
2MnO +5H2C2O4+6H+===2Mnx++10CO2↑+8H2O
+5H2C2O4+6H+===2Mnx++10CO2↑+8H2O
则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________ mg/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
B.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大
C.Ca(HCO3)2溶液与过量NaOH溶液反应可得到Ca(OH)2
D.25 ℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气是清洁燃料,其燃烧产物为________。
(2)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为__________________________________________,反应消耗1 mol NaBH4时转移的电子数目为________。
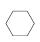 (3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
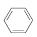 (g)
(g) 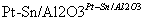 (g)+3H2(g)。
(g)+3H2(g)。
在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=________。
(4)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。

①导线中电子移动方向为________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。(η=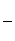 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________________________。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是________________________________________________________________________
________________________________________________________________________。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图像,模型见图。下列关于水的说法正确的是( )

A.水是弱电解质
B.可燃冰是可以燃烧的水
C.氢氧两种元素只能组成水
D.0 ℃时冰的密度比液态水的密度大
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钾是工业生产和实验室的重要氧化剂。工业上常用铬铁矿(主要成分为FeO·Cr2O3,以及SiO2、Al2O3等杂质)为原料生产。实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下:

图K52
反应器中主要发生的反应为
Ⅰ.FeO·Cr2O3+NaOH+KClO3→Na2CrO4+Fe2O3+H2O+KCl(未配平);
Ⅱ.Na2CO3+SiO2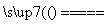 Na2SiO3+CO2↑;
Na2SiO3+CO2↑;
Ⅲ.Al2O3+2NaOH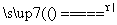 2NaAlO2+H2O。
2NaAlO2+H2O。
在步骤③中将溶液的pH调节到7~8,可以将SiO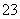 和AlO
和AlO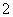 转化为相应的沉淀除去。
转化为相应的沉淀除去。
(1)在反应Ⅰ中氧化剂是________,若有245 g KClO3参加反应,则转移的电子数为______________________。
(2)反应器中生成的Fe2O3又可和Na2CO3反应得到一种摩尔质量为111 g/mol的化合物,该化合物能剧烈水解,在操作②中生成沉淀而除去。写出生成该化合物的化学反应方程式:________________________________。
(3)操作④的目的是将CrO 转化为Cr2O
转化为Cr2O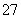 ,其现象为____________________,离子方程式为________________________________________________________________________
,其现象为____________________,离子方程式为________________________________________________________________________
________________________________________________________________________。
(4)请选用合适的方法进一步提纯粗产品重铬酸钾______(填字母)。
A.重结晶 B.萃取分液
C.蒸馏
(5)分析产品中K2Cr2O7的纯度是利用硫酸酸化的K2Cr2O7将KI氧化成I2,然后利用相关物质测出I2的量从而获得K2Cr2O7的量。写出酸化的K2Cr2O7与KI反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制乙烯时,常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
(1)请用表中编号为①、②、③、④的装置设计一个实验,以验证上述反应混合气体中含CO2、SO2和水蒸气。用装置的编号表示装置的连接顺序(按产物气流从左到右顺序):________→________→
________→________。
(2)实验时装置①中A瓶的现象是________,原因是________。B瓶中的现象是________,B瓶溶液的作用是________。若C瓶中品红溶液不褪色,说明________。
(3)装置③中加的固体药品是________,以验证混合气体中有________。装置②中盛的溶液是________,以验证混合气体中的________。
(4)装置①在整套装置中所放位置的理由是____________。
| 编号 | ① | ② | ③ | ④ |
| 装置 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式__________________________________________
________________________________________________________________________。
(2)某无色溶液只含有下列8种离子中的某几种:Na+、H+、Mg2+、Ag+、Cl-、OH-、HCO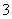 、NO
、NO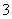 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则:
①该溶液与Al2O3反应后有Al3+生成,则原溶液中一定含有________,一定不会含有大量的________。
②该溶液与Al2O3反应后有AlO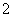 生成,则原溶液中一定含有________,可能含有大量的________。
生成,则原溶液中一定含有________,可能含有大量的________。
③写出该溶液与Al2O3反应生成AlO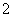 的离子方程式
的离子方程式
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com