
| A、降低体系的温度 |
| B、增大容器的体积 |
| C、体积不变充入N2 |
| D、将NH3及时移走 |


科目:高中化学 来源: 题型:
| A、某温度时,1L pH=6的纯水,含10-6mol OH-离子 |
| B、含10.6g Na2CO3溶液中,所含阴离子总数等于0.1mol |
| C、1L 1mol/L FeCl3溶液中,若Fe3+离子数目为1mol,则Cl-离子数目大于3mol |
| D、电解精炼粗铜时,每转移1mol电子,阳极上溶解的Cu原子数必为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑ |
| B、少量CO2通入苯酚钠溶液中:C6H5O-+CO2+H2O═C6H5OH+HCO3- |
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、向氨水中通入少量的二氧化硫气体:2NH3?H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然气燃烧提供热量 |
| B、氯水使红色纸张褪色 |
| C、钢铁制品在空气中被腐蚀 |
| D、二氧化硫通人品红溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的摩尔质量不再变化 |
| B、容器内气体压强不再变化 |
| C、混合气体的颜色不再变化 |
| D、混合气体的密度恒定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
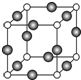 已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子价电子构型为:nsnnpn;钠在W的单质中燃烧生成淡黄色固体;K位于ds区且原子的最外层电子数与X的相同.请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子价电子构型为:nsnnpn;钠在W的单质中燃烧生成淡黄色固体;K位于ds区且原子的最外层电子数与X的相同.请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C |
①能使溴的四氯化碳溶液褪色; ②比例模型为: 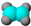 ③能与水在一定条件下反应生成C |
①由C、H两种元素组成; ②球棍模型为: 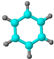 |
①由C、H、O三种元素组成; ②能与Na反应; ③其相对分子质量为46. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com