
��һ���¶��·�����Ӧ��I2(g)+H2(g)  2HI(g)�� ��H<0����ƽ�⡣HI���������
2HI(g)�� ��H<0����ƽ�⡣HI���������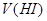 ��ʱ��仯��ͼ���ߣ�II����ʾ�����ı䷴Ӧ�������ڼ�������
��ʱ��仯��ͼ���ߣ�II����ʾ�����ı䷴Ӧ�������ڼ�������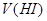 �ı仯�����ߣ�I����ʾ������������
�ı仯�����ߣ�I����ʾ������������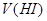 �ı仯�����ߣ�III����ʾ������������������ֱ���
�ı仯�����ߣ�III����ʾ������������������ֱ���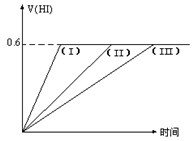
�ٺ��������£������¶� �ں��������£������¶�
�ۺ��������£���С��Ӧ������� �ܺ��������£�����Ӧ�������
�ݺ��º��������£������ʵ��Ĵ���
| A���٢ݣ��� | B���ڢݣ��� | C���ۢݣ��� | D���ۢݣ��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1mol H2��g����2molI2��g������2L�ܱ������У���һ���¶��·�����Ӧ��H2��g��+I2��g��?
��1mol H2��g����2molI2��g������2L�ܱ������У���һ���¶��·�����Ӧ��H2��g��+I2��g��?�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1mol I2��g����2mol H2����5L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2��g��?2HI��g����H��0�����ﵽƽ�⣮HI���������w��HI����ʱ��仯�����ߣ�����ʾ��
��1mol I2��g����2mol H2����5L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2��g��?2HI��g����H��0�����ﵽƽ�⣮HI���������w��HI����ʱ��仯�����ߣ�����ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1molH2��g����2mol I2��g������ij2L�ܱ������У���һ���¶��·�����Ӧ��
��1molH2��g����2mol I2��g������ij2L�ܱ������У���һ���¶��·�����Ӧ�� 2HI��g��+Q��Q��0�������ﵽƽ�⣬HI����������أ�HI����ʱ�䣨t���仯��ͼ������ʾ�����ı䷴Ӧ�������أ�HI���ı仯������ͼ��I����ʾ����ı�����������ǣ�������
2HI��g��+Q��Q��0�������ﵽƽ�⣬HI����������أ�HI����ʱ�䣨t���仯��ͼ������ʾ�����ı䷴Ӧ�������أ�HI���ı仯������ͼ��I����ʾ����ı�����������ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪298Kʱ��
��֪298Kʱ��| c |
| 2 |
| c |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
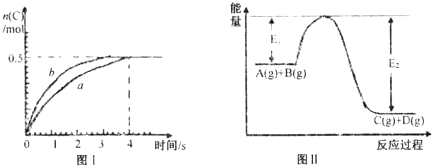
| A���˷�Ӧ�����е������仯������ͼII��ʾ | B�����¶��£��÷�Ӧ��ƽ�ⳣ����ֵΪ1 | C���÷�Ӧ4s��ƽ������v��A��=0.125mol?L-1?s-1 | D�����ں��¼Ӵ�Ӧ�������ݻ������£��÷�Ӧ����b���߽��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com