(2012?闸北区一模)

(1)选用方案I时,X应该具有的性质是
有挥发性(或易升华)
有挥发性(或易升华)
,残留物应该具有的性质是
受热不挥发,且具有较高的热稳定性
受热不挥发,且具有较高的热稳定性
;
(2)选用方案Ⅱ从某黑色粉末(含有MnO
2和CuO)中分离X(MnO
2),加入的试剂是
稀盐酸(或稀硫酸 或稀硝酸)
稀盐酸(或稀硫酸 或稀硝酸)
;
王同学参照以上方案I和Ⅱ,设计以下实验方案除去AlCl
3固体中的FeCl
3.
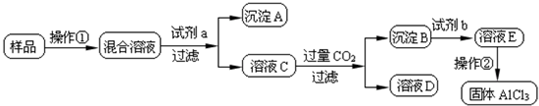
(3)操作①所需的玻璃仪器为
烧杯、玻璃棒
烧杯、玻璃棒
;
(4)试剂a为
过量的氢氧化钠(氢氧化钾)溶液
过量的氢氧化钠(氢氧化钾)溶液
;试剂b为
适量的盐酸
适量的盐酸
;
(5)请描述操作②的步骤:
将溶液加热浓缩,然后冷却浓溶液,过滤即可得到固体氯化铝
将溶液加热浓缩,然后冷却浓溶液,过滤即可得到固体氯化铝
;
(6)李同学认为在溶液C中滴加适量的试剂b就能得到溶液E,从而得到AlCl
3固体,你
不赞同
不赞同
(填“赞同”或“不赞同”)李同学,理由是
会在氯化铝溶液中引入氯化钠杂质
会在氯化铝溶液中引入氯化钠杂质
.




