
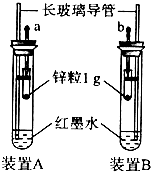
 某化学兴趣小组按图示装好了实验装置,一支胶头滴管盛有盐酸,另一支胶头滴管盛有同体积、同浓度的醋酸.实验时同时完全捏扁a、b的胶头,观察实验现象.
某化学兴趣小组按图示装好了实验装置,一支胶头滴管盛有盐酸,另一支胶头滴管盛有同体积、同浓度的醋酸.实验时同时完全捏扁a、b的胶头,观察实验现象.

科目:高中化学 来源:2011-2012年山东省潍坊市三县高一上学期模块学分认定检测化学试卷 题型:选择题
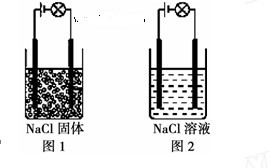
某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是
A. NaCl是非电解质
B. NaCl溶液是电解质
C. NaCl在水溶液中电离出了可以自由移动的离子
D. NaCl溶液中水电离出大量的离子
查看答案和解析>>
科目:高中化学 来源:2014届山东省高一12月学情调研考试化学试卷 题型:选择题
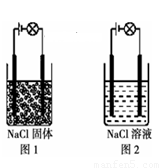
某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是
A. NaCl是非电解质
B. NaCl溶液是电解质
C. NaCl在水溶液中电离出了可以自由移动的离子
D. NaCl溶液中水电离出大量的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
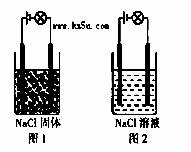
某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是
A. NaCl是非电解质
B. NaCl溶液是电解质
C. NaCl在水溶液中电离出了可以自由移动的离子
D. NaCl溶液中水电离出大量的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是
A. NaCl是非电解质
B. NaCl溶液是电解质
C. NaCl在水溶液中电离出了可以自由移动的离子
D. NaCl溶液中水电离出大量的离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com