
| A. | 海水中含有溴元素,只需经过化学变化就可以得到高纯度的溴 | |
| B. | 海水淡化涉及到了化学变化 | |
| C. | 从海水中可以得到NaCl,除了食用外,还可以用于工业制氯气 | |
| D. | 海水中含有丰富的钠、镁、碘、金 |
分析 A.将溴离子氧化成溴单质后,还需要通过萃取、蒸馏等物理方法分离出溴;
B.蒸馏法获得蒸馏水的过程中,没有涉及化学变化;
C.氯化钠可以加工变成食盐,也可以在工业上通过电解熔融饱和氯化钠溶液获得氯气;
D.海水中不含有丰富的金元素.
解答 解:A.海水中含有溴元素,经过化学变化将溴离子氧化成溴单质后,还需要通过物理变化分离出溴,如:萃取、分液、蒸馏等操作,故A错误;
B.通过蒸馏操作实现海水的淡化过程中,发生的是物理变化,没有涉及化学变化,故B错误;
C.从海水中得到氯化钠后,既可以使用,还可通过饱和食盐水的方法获得氢氧化钠和氯气,故C正确;
D.海水中含有丰富的钠、镁、碘等元素,但是不含有丰富的金,故D错误;
故选C.
点评 本题主要海水资源的利用,题目难度中等,侧重于考查学生基本知识和基本反应原理的掌握,注意掌握海水资源的综合应用方法,明确海水淡化的方法、物理变化与化学变化区别为解答关键.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题
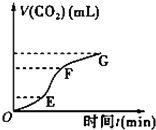 用纯净的碳酸钙跟稀盐酸反应制取二氧化碳气体.请回答问题:
用纯净的碳酸钙跟稀盐酸反应制取二氧化碳气体.请回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | O2 | C. | NO2和O2 | D. | NO和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 只有非金属原子间才能形成共价键 | |
| C. | 由共价键形成的一定是共价化合物分子 | |
| D. | 熔化后不导电的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和H2S | B. | O2和NH3 | C. | CO2和H2 | D. | CH4和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1molP4含有p-p键的个数为4NA | |
| B. | 1molSiC中含有C-Si键的个数为2NA | |
| C. | 含C为1mol的金刚石中含有C-C键的个数为2NA | |
| D. | 1molSi02中含Si-O键的个数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com