
2011年7月21日,世界各国领导人在南非德班共同商讨应对气候变化的道路——“拯救人类的最后机会”。要想节能减排下列属最有希望的新能源是( )
①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③④⑤⑥ D.除①②外
 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2016-2017学年天津静海一中等六校高一上期中化学卷(解析版) 题型:选择题
下列关于胶体的叙述不正确的是( )
A.胶体区别其他分散系的本质特征是分散质的微粒直径在10﹣9~10﹣7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够使水中悬浮的固 体颗粒沉降,达到净水目的
体颗粒沉降,达到净水目的
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:实验题
有同学探究了三价铁离子在水溶液中的一些反应:
I、甲组同学将氯化铁溶液滴加到碘化钾溶液中,发 现溶液的颜色变为浅绿色,请写出此反应的离子方程式 。同学们经过测定、查阅资料得出了以下结论:正向反应速率和I-、Fe3+的浓度关系为υ=k[I-]m[Fe3+]n(k为常数)
现溶液的颜色变为浅绿色,请写出此反应的离子方程式 。同学们经过测定、查阅资料得出了以下结论:正向反应速率和I-、Fe3+的浓度关系为υ=k[I-]m[Fe3+]n(k为常数)
[I-](mol·L-1) | [Fe3+ ]( mol·L-1) | υmol·L-1·s-1) | |
(1) | 0.20 | 0.80 | 0.032k |
(2) | 0.60 | 0.40 | 0.144k |
(3) | 0.80 | 0.20 | 0.128k |
通过所给数据计算得知:
(1)在υ=k[I-]m[Fe3+]n中,m、n的值为m=_________,n=_______ __。
__。
(2)碘离子浓度对反应速率的影响___________铁离子浓度对反应速率的影响。(选填:小于、大于、等于)。
II、乙组同学将硫氰化钾溶液滴入至氯化铁溶液中,得到了红色液体。
(1)在溶液中加入硫氰化钾粉末少量,颜色将 (填“变深”、“变浅”、“无明显现象”)。
(2)在溶液中加入氯化钾粉末少量,颜色将 (填“变深”、“变浅”、“无明显现象”)。
请用离子方程式解释原因: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
反应Fe(s)+CO2(g) FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是( )
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是( )
A.升高温度该反应的正反应速率增大,逆反应速率减小
B.该反应的化学平衡常数表达式为K=
C.该反应的正反应是吸热反应
D.增大CO2浓度,平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
下列关于化学平衡的说法中正确的是( )
A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,正反应速率和逆反应速率相等都等于0
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
D.化学平衡不可以通过改变条件而改变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
下列各图示中能较长时间看到Fe(OH)2白色沉淀的是
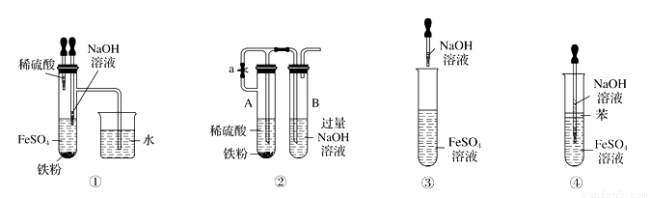
A.①②③ B.①②④ C.①②③④ D.②③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(x)与溶液中沉淀物的量(y)的关系示意图正确的是( )
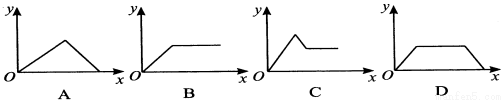
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
下列化学变化中,需加入氧化剂才能实现的是 ( )
A.C→CO2 B.CO2→ CO C.CuO→Cu D.H2SO4→BaSO4
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷(解析版) 题型:填空题
氮氧化物(NOx)种类很多,造成大气污染的主要是NO和NO2,研究它们的综合利用有重要意义。
(1)NO可通过氧化-还原法转化为N2,转化关系如下:
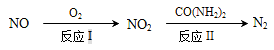
反应Ⅰ的化学方程式是_______;反应Ⅱ的还原剂是_______。
(2)NO还可与C在一定条件下反应得到无污染的气 体。NO与C在一定条件下反应的化学方程式是_______。
体。NO与C在一定条件下反应的化学方程式是_______。
(3)NO也可直接用活性铁粉转化为N2。
已知:N2(g)+O2(g)=2NO(g) △H1
4Fe(s)+3O2(g)=2Fe2O3(s) △H2
则6NO(g)+4Fe(s)=2Fe2O3(s)+3N2(g) △H =___________(用“△H1”、“△H2”表示)。
(4)NO2可电解制备绿色硝化试剂N2O5。下图是其原理示意图。
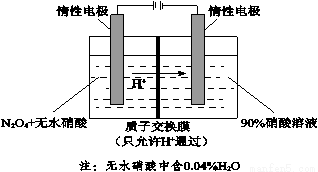
① 阳极电解液中的N2O4由NO2降温转化得到,降温的原因是_______________。
② 阳极区生成N2O5的电极反应式是_______________。
③ 阴极区得到一种可循环利用的物质,其化学式是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com