
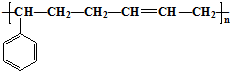 合成这种橡胶的单体应是( )
合成这种橡胶的单体应是( )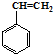 ②
②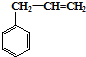 ③CH3-CH=CH-CH3④CH≡C-CH3⑤CH2=CH-CH=CH2.
③CH3-CH=CH-CH3④CH≡C-CH3⑤CH2=CH-CH=CH2.| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ①⑤ |
分析 解答此类题目,首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,丁苯橡胶为加聚产物,
加聚产物的单体推断方法:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换.
解答 解:该高聚物链节主链不含杂原子,属于加聚反应生成的高聚物,链节主链上存在碳碳双键结构,有6个碳原子,其单体必为两种,按如图所示断开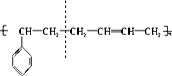 ,在将双键中的1个c-c打开,然后将半键闭合即可的该高聚物单体是①
,在将双键中的1个c-c打开,然后将半键闭合即可的该高聚物单体是① ⑤CH2=CH-CH=CH2,
⑤CH2=CH-CH=CH2,
故选D.
点评 本题考查聚合物寻找单体的方法,注意聚合反应的类型来分析,题目难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | 制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞 | |
| B. | 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷气体的纯度 | |
| C. | 实验时将所有的废气通过通风橱排出实验室,以免污染实验室 | |
| D. | 给试管中的液体加热时不时移动试管或加入碎瓷片,以免暴沸伤人 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH=CH2与HCl加成 | |
| B. | C6H5-CH3在铁粉存在下与氯气反应 | |
| C. | CH3-CH2-CHBr-CH3在氢氧化钠乙醇溶液中加热反应 | |
| D. | CH3-CHOH-CH3在浓硫酸存在下,发生分子内脱水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.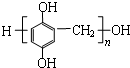 单体是
单体是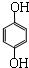 和HCHO,聚合物
和HCHO,聚合物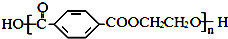 单体是HOCH2CH2OH、
单体是HOCH2CH2OH、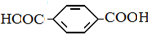
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种 | |
| B. | 戊二醛能在加热条件下和新制备的氢氧化铜反应 | |
| C. | 戊二醛不能使酸性KMnO4溶液褪色 | |
| D. | 2%的GA溶液能破坏菌体蛋白质,杀死微生物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,基态原子核外电子排布式1s22s22p63s23p63d24s2.该元素的原子序数为22,该元素是金属元素(填“金属”或“非金属”).
,基态原子核外电子排布式1s22s22p63s23p63d24s2.该元素的原子序数为22,该元素是金属元素(填“金属”或“非金属”).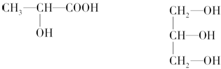
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com