
下列说法正确的一组是( )
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②盐都是强电解质
③0.5 mol·L-1的所有一元酸中氢离子浓度都是0.5 mol·L-1
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电
A.①③⑤⑥ B.②④⑤⑥
C.只有⑤ D.只有⑥
科目:高中化学 来源: 题型:
将0.5L 1mol/L FeCl3溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是()
A. 3mol/L B. 2mol/L C. 1.5mol/L D. 1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同体积同质量的CO2、CO、H2、O2的压强,按从大到小的顺序排列正确的是()
A. H2>O2>CO>CO2 B. H2>CO>O2>CO2 C. CO2>O2>CO>H2 D. CO2>H2>O2>CO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中,发生消去反应生成的烯烃只有一种的是( )
①2丁醇 ②2甲基2丙醇
③1丁醇 ④2甲基2丁醇
A.①② B.②③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为1 mol·L-1。下面四个选项中能达到此目的的是( )
A.Na+、K+、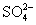 、Cl-
、Cl-
B.Cu2+、K+、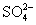 、
、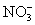
C.H+、K+、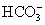 、Cl-
、Cl-
D.Mg2+、Na+、Cl-、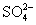
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |
|
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B ,D 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为 。
(3)C常用作净水剂,用离子方程式表示其净水原理 。
(4)在A溶液中加入少量澄清石灰水,其离子方程式为 。
(5)向20 mL 2 mol·L-1C溶液中加入30 mL E溶液,充分反应后得到0.78 g沉淀,则E溶液的物质的量浓度可能是 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
在1~18号元素中,部分连续元素单质的熔点情况如下图所示,试回答:
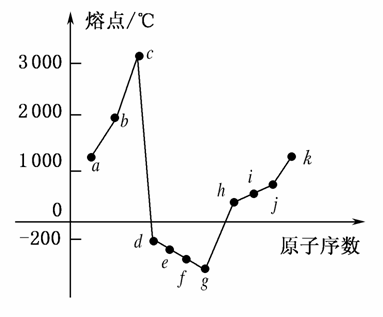
(1)c点代表的单质可以是________,其熔点高的主要原因是____________________________。
(2)d所属的晶体类型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) 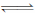 CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g) +H2(g);ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
A.增加碳的用量
B.升高温度
C.用CO吸收剂除去CO
D.加入催化剂
(2)已知,C(s)+ CO2(g)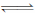 2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)
2CO(g);ΔH=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)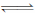 CO2(g)+H2(g)的ΔH= kJ•mol-1。
CO2(g)+H2(g)的ΔH= kJ•mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)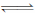 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其他条件不变,降低温度,达到新平衡前v(逆)_____v(正)(填“>”、“<”或“=”)。
②该温度下,此反应的平衡常数K= 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com