
| A、某物质的溶液pH<7,则该物质属于酸或强酸弱碱盐 |
| B、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
| D、AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |


科目:高中化学 来源: 题型:
| ||
| 高温高压 |
| A、N2、NH3、H2三种物质的浓度一定相等 |
| B、N2、H2全部变成NH3 |
| C、反应混合物各组分的浓度不再变化 |
| D、反应已经停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Ba2+、Cl-、HCO3- |
| B、Na+、K+、SO42-、Cl- |
| C、K+、Na+、Ba2+、Cl- |
| D、SO42-、CH3COO-、Al3+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、没有水就没有生命 |
| B、饮用水越纯净越好 |
| C、养成良好的饮食习惯,只吃蔬菜,水果等碱性食物 |
| D、调味剂和营养剂加的越多越好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序:r(B)>r(C)>r(A) |
| B、元素E的氧化物的水化物一定是强酸 |
| C、D单质在一定条件下可以与氧化铁发生置换反应 |
| D、工业上常用电解元素C、D的氯化物来制取它们的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
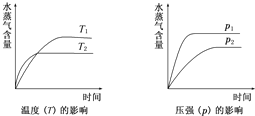
| A、CO2(g)+H2(g)?CO(g)+H2O(g);△H>0 |
| B、CO2(g)+2NH3(g)?CO(NH2)2(s)+H2O(g);△H<0 |
| C、CH3CH2OH(g)?CH2=CH2(g)+H2O(g);△H>0 |
| D、2C6H5CH2CH3(g)+O2(g)?2C6H5CH═CH2(g)+2H2O(g);△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
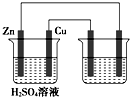 如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )
如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )| A、铜在原电池中作负极,在电镀池中作阳极 |
| B、原电池溶液增加的质量比电镀池阴极增加的质量大 |
| C、锌棒每减少0.65 g,导线上转移的电子约为1.204×1022个 |
| D、电路中电子的移动方向是从Zn沿导线到电镀池的铜极,再经过溶液到铁棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol/L |
| B、0.6 mol/L |
| C、1 mol/L |
| D、2 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com