
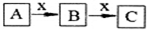 A、B、C、x均为中学化学常见物质,且A、B、C含有同一种元素,在一定条件下发生如图所示的化学变化.则x不可能是( )
A、B、C、x均为中学化学常见物质,且A、B、C含有同一种元素,在一定条件下发生如图所示的化学变化.则x不可能是( )| A. | C | B. | Al | C. | Fe | D. | O2 |
分析 A、B、C、X均为中学化学常见物质,且A、B、C含有同一种元素,A能连续与同一种物质反应,如果X是单质,则组成X元素可能属于变价元素,据此分析解答.
解答 解:A.如果X是C,则A可以为氧气,氧气和C反应生成B为二氧化碳、二氧化碳和C反应生成C为CO,符合题中图示,故A不选;
B.Al的正化合价只有一种,没有符合条件的能和Al连续发生反应的物质,故B选;
C.如果X是铁,则A可以是氯气,氯气和铁反应生成氯化铁,氯化铁和铁反应生成氯化亚铁,符合题中图示,故C不选;
D.如果X是氧气,则A可以是碳,碳和氧气反应生成CO、CO和氧气反应生成二氧化碳,A也可以是Na,钠和氧气反应生成氧化钠、氧化钠和氧气反应生成过氧化钠,符合题中图示,故D不选;
故选B.
点评 本题考查元素化合物推断,为高频考点,侧重考查学生发散思维能力,可以采用代入法分析解答,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 早在1000多年前,我国就已采用加热胆矾(CuSO4•5H2O)或绿矾(FeSO4•7H2O) 的方法制硫酸,尽管硫酸的生产工艺几经改进,此方法仍然是工业生产硫酸的主要方法 | |
| B. | 氢能是未来能源结构中最具发展潜力的清洁能源之一.目前已有专家已研究出用淀粉或纤维素与水在酶作用下转变为二氧化碳和氢气的方法制氢气.从整个循环来看,利用该方法得到的氢能来源于太阳能 | |
| C. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是:CH3C≡CH+CO+CH3OH$\stackrel{Pd}{→}$CH2=C(CH3) COOCH3,其过程符合绿色化学的原则 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维中所用材料为晶体硅 | |
| B. | SiO2是酸性氧化物,所以不与任何酸反应 | |
| C. | 可用Na2SiO3溶液和CO2反应来制备H2SiO3 | |
| D. | NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下表各组物质中,物质之间不可能实现如图所示转化的是:
下表各组物质中,物质之间不可能实现如图所示转化的是:| 选项 | X | Y | Z | M |
| A | FeS2 | SO2 | SO3 | O2 |
| B | NaOH | Na2CO3 | NaHCO3 | CO2 |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | AlO2- | Al(OH)3 | Al3+ | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .实验室制取并检验气体A的方法是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则是氨气.
.实验室制取并检验气体A的方法是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则是氨气.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内X、Y、Z的速率之比为1:2:2 | |
| B. | 单位时间生成0.1 mol X的同时生成0.2 mol Z | |
| C. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| D. | 容器内气体密度不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇 | B. | 乙醇 | C. | 乙二醇 | D. | 丙三醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com