

 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.1 | B.2 | C.3 | D.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | ② | ③ | ④ | |
| 3 | | ⑤ | ⑥ | ⑦ | | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与水或酸反应置换氢气的难易 | B.金属性的强弱 |
| C.氢氧化物的碱性 | D.氧化性的强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性强弱: HI > HBr > HCl > HF | B.原子半径大小: Na > S > O |
| C.碱性强弱: KOH > NaOH > LiOH | D.还原性强弱: F- > Cl- > I- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||||
| 1 | ① | | | | | | | | ||||||
| 2 | | | | ② | ③ | | ④ | | ||||||
| 3 | | ⑤ | ⑥ | | | ⑦ | ⑧ | ⑨ | ||||||
| 4 | ⑩ | | | | | | ⑾ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在元素周期表中,s区,d区和ds区的元素都是金属 |
| B.在元素周期表中,每个纵列的价电子层的电子总数一定相等 |
C.某基态原子错误的核外电子排布图为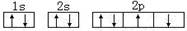 ,该排布图违背了泡利原理 ,该排布图违背了泡利原理 |
| D.在氢原子的基态电子的概率分布图中,小黑点的疏密程度表示电子在该区域空间出现概率的大小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com