
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | NaOH固体溶解后立即转入容量瓶 | |
| C. | 在容量瓶中进行定容时仰视刻度线 | |
| D. | 定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度 |
科目:高中化学 来源: 题型:选择题
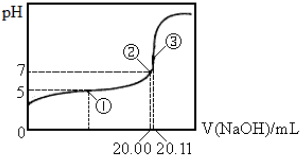
| A. | 该温度下CH3COOH的电离平衡常数Ka=2.0×10-5 | |
| B. | ③点所示溶液中:c(CH3C00-)+c(CH3C00H)=(Na+)+c(0H-) | |
| C. | 该醋酸的浓度为0.1006mol•L-1 | |
| D. | 由图示可以计算醋酸钠的水解平衡常数为5.0×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4+2NaHCO3═2NaCl+2H2O+2CO2↑ | B. | 2HCl+BaS═BaCl2+H2S↑ | ||
| C. | CO2+H2O+Ca(ClO)2═CaCO3↓+2HClO | D. | H2S+CuSO4═CuS↓+H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海带 | B. | 食盐 | C. | 面粉 | D. | 酸奶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
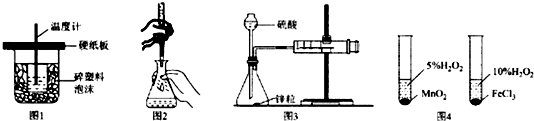
| A. | 图1装置用于中和热的测定 | |
| B. | 图2装置用于高锰酸钾溶液滴定草酸 | |
| C. | 图3装置用于测定氢气的反应速率(单位mL/s) | |
| D. | 图4装置用于研究不同催化剂对反应速率的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com