
【题目】已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是
A. Y和Z可以组成元素质量比为7:16的化合物
B. X和Y可以组成原子个数比分别为3:l和2:l的两种化合物
C. 由X、Y、Z三种元素中任意两种组成的具有10电子的微粒多于2种
D. X、Y、Z只能组成一种盐,其中X、Y、Z原子个数比为4:2:3
【答案】D
【解析】X、Y、Z都是短周期元素,它们的原子序数依次递增,Z原子的最外层电子数是次外层的3倍,则Z是O元素;X原子的电子层数与它的核外电子总数相等,且原子序数小于Z,所以X是H元素;Y和Z可以形成两种以上气态化合物,且Y的最外层上电子数比Z的最外层上电子数少1,且Y的原子序数小于Z,所以Y是N元素;A.Y是N元素,Z是O元素,Y和Z的质量比为7:16时其原子个数比=![]() =1:2,该化合物是NO2,故A正确;B.X和Y可以组成NH3、N2H4两种化合物,它们原子个数之比分别为3::2:1,故C正确;C.由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有H2O、H3O+、NH3、NH4+,故C正确;D.X、Y、Z可以组成一种盐,当X、Y、Z元素原子个数之比为4∶2∶3时,该盐是NH4NO3,但还可能组成NH4NO2,故D错误;故选D。
=1:2,该化合物是NO2,故A正确;B.X和Y可以组成NH3、N2H4两种化合物,它们原子个数之比分别为3::2:1,故C正确;C.由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有H2O、H3O+、NH3、NH4+,故C正确;D.X、Y、Z可以组成一种盐,当X、Y、Z元素原子个数之比为4∶2∶3时,该盐是NH4NO3,但还可能组成NH4NO2,故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】下列方法中,可制得Cl2的正确组合是( )
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热 ③NaClO和浓盐酸混合 ④K2Cr2O7和浓盐酸混合 ⑤KClO3和浓盐酸混合共热 ⑥KMnO4和浓盐酸混合
A. ①②⑥ B. ②④⑥
C. ①④⑥ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程能量变化如下所示:H2(g)+Cl2(g)===2HCl(g) ΔH
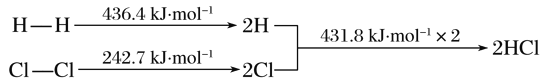
下列说法错误的是( )
A. H—H键比Cl—Cl键稳定
B. 正反应活化能比逆反应活化能高
C. ΔH=-184.5 kJ·mol-1
D. 在相同条件下,1 mol H2(g)和1 mol Cl2(g)分别在点燃和光照条件下反应生成2 mol HCl(g),重新恢复到原来的状态时ΔH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿斯巴甜(F)是一种广泛应用于食品、饮料、糖果的甜味剂,其结构式为 ,合成阿斯巴甜的一种合成路线如下:
,合成阿斯巴甜的一种合成路线如下:

已知:①芳香族化合物A能发生银镜反应,核磁共振氢谱显示有5 种不同化学环境的氢。
②
③RCN ![]() RCOOH
RCOOH
④
回答下列问题:
(1)A 的名称为_________,E含有的官能团是_____________。
(2)反应①的类型是_________,反应⑤的类型是__________。
(3)C和D的结构简式分别是_______、_________。
(4)C的同分异构体中能同时满足下列条件的共有________种(不考虑立体异构)。
①苯环上有两个取代基
②能与FeCl3 溶液作用显紫色
③能与饱和NaHCO3 溶液反应产生气体
(5)参照上述合成路线,设计一条由甲醛为起始原料制备氨基乙酸的合成路线:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成。回答下列问题:

(1)B和A为同系物,则 B 的加聚产物的结构简式为________;
(2)反应①的化学方程式为 __________________;
(3)反应③的化学方程式为__________________;反应类型为__________________。
(4)反应②的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙烯醇(CH2=CHOH)不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物,现有1mol乙二醇在一定条件下脱去1molH2O,所得产物的结构简式有下列几种,其中不可能的是
①CH2=CH2 ②![]() ③CH3CHO ④
③CH3CHO ④![]() ⑤
⑤![]()
A. 只有① B. 只有①④ C. 只有①⑤ D. 只有①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。稀土元素有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,位于周期表的_____区,基态原子价电子排布图为_______。
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有_______。
(3)Sm(钐)的单质与l,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子杂化轨道类型为______, lmol CH2=CH2中含有的σ键数目为______。常温下l,2-二碘乙烷为液体而乙烷为气体,其主要原因是__________。
(4) PrO2(二氧化镨)的晶体结构与CaF2相似,晶饱中Pr(镨)原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有________个氧原子。
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。晶胞中Ce(铈)原子的配位数为_______,列式表示Ce(铈)单质的密度:________g/cm3(用NA表示阿伏伽德罗常数的值,不必计算出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com