
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高呼口号:钓鱼岛,中国的! |
| B、高举鲜艳的五星红旗,齐唱国歌 |
| C、焚烧像征日本军国主义的画像 |
| D、极个别丧失理智的人违法打砸同胞的日系车 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某固体中加入稀盐酸,产生了无色气体,证明该固体一定含有CO32- |
| B、某无色溶液滴加酚酞试液显红色,该溶液不一定是碱 |
| C、某溶液中滴加了BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42- |
| D、验证碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加AgNO3,有白色沉淀出现证明含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
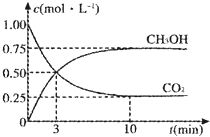 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.| 光合作用 |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com