
将纯水加热至较高温度,下列叙述正确的是 ( )
A.水的离子积变大、pH变小、呈酸性 B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性 D.水的离子积变大、pH变小、呈中性
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
关于FeCl3进行的实验,下列预测正确的是( )
| 选项 | 实验 | 预测 |
| A | 蒸发FeCl3溶液 | 得到FeCl3固体 |
| B | 在FeCl3、CuCl2混合液中,加入少量Fe粉 | 一定有H2产生且有Cu析出 |
| C | 用FeCl3固体溶于水配制饱和溶液 | 会有Fe(OH)3沉淀产生 |
| D | 在FeCl3溶液中加入KHCO3溶液 | 有CO2产生,但无Fe(OH)3沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同回答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。
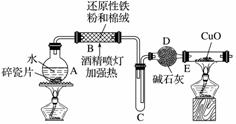
(1)硬质玻璃管B中发生反应的化学方程式为__________________________________。
(2)反应前A中投放碎瓷片的目的是___________________________________________。
(3)装置E中的现象是______________________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变血红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为________。
①一定有Fe3O4 ②一定有Fe
③只有Fe3O4 ④只有Fe
(6)另一份用__________(填仪器名称)加入________(填试剂和现象),可以证明溶液中存在Fe2+。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
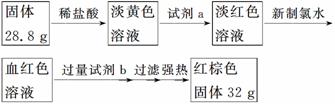
(7)试剂b的化学式是________。
(8)计算反应后B装置中铁元素的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知植物油的组成元素只有C、H、O三种,某科研机构指出:将植物油代替汽油做汽车的燃料具有战略意义,这项研究已经取得了实质性进展,并已经开始试用,这对于汽油价格居高不下是一个很大的冲击,对消费者来说是一个很好的消息。据以上信息,下列有关植物油代替汽油的说法错误的是
( )。
A.使用植物油代替汽油作燃料有助于减轻大气污染,改善大气环境
B.推广使用植物油代替汽油可在一定程度上缓解当前能源紧张的形势
C.植物油是一种二级能源,与汽油相似,也是一种不可再生能源
D.使用植物油代替汽油有利于调整产业结构、增加农民收入、促进经济发展
查看答案和解析>>
科目:高中化学 来源: 题型:
杜邦公司因发明了一项新技术而获得2003年美国总统绿色化学奖,该技术利用基因工程将酵母菌的基因引入一种大肠杆菌,用来将葡萄糖发酵生成1,3丙二醇(HOCH2CH2CH2OH)。
(1)在上述发酵过程中,葡萄糖首先转化为二羟基丙酮的一磷酸酯,随后转化为目标产物。该反应对葡萄糖的原子利用率为 。(原子利用率是目标产物的相对分子质量除以反应物相对原子质量之和乘以100%)
(2)生产1,3丙二醇的传统工艺是以石油为原料按下述路线进行的:石油→乙烯→环氧乙烷→3羟基丙醛→1,3丙二醇。获得3羟基丙醛的反应在乙醚溶剂中进行,用钴或铑作催化剂,温度为80 ℃,压强为107Pa;后一反应用镍作催化剂,温度为80~1 200 ℃,压强为1.6×107Pa。对比之下,新工艺至少具有哪些绿色化学特征?
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL浓度为2mol/L的盐酸跟过量的锌片反应,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是 ( )
A.加入适量的6mol/L的盐酸 B.加入数滴氯化铜溶液
C.加入适量醋酸钠固体 D.加入适量的氯化钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1mol/L的CH3COOH溶液中存在如下电离平衡: ( )
CH3COOH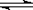 CH3COO-+H+ ,对于该平衡,下列叙述正确的是
CH3COO-+H+ ,对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向正反应方向移动
B.加水,反应速率增大,平衡向逆反应方向移动
C.滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
高炉炼铁中发生的基本反应如下: FeO(s)+CO(g) 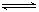 Fe(s)+ CO2(g)已知1100℃,K=0.263
Fe(s)+ CO2(g)已知1100℃,K=0.263
(1) 1100℃时,若平衡向右进行,高炉内CO2和CO的体积比值 。(填“增大”“减小”或“不变”)
(2)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态 (填“是”或“否”),此时化学反应速率是V正 V逆(填“大于”、“小于”或“等于”),其原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于苯的叙述正确的是( )
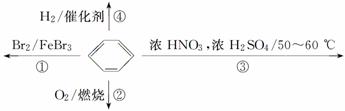
A.反应①为取代反应,有机产物与水混合浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为一个苯分子含有三个碳碳双键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com