
据报道,某些花岗岩会产生氡(22286Rn),这是一种放射性很强的原子,会对人体产生伤害,因此,家庭装修时应尽量避免使用天然产的花岗岩材料。已知氡是一种稀有气体元素,下列叙述正确的是( )
A.该原子与同周期ⅠA.ⅡA族阳离子具有相同的核外电子层结构
B.该原子最外层有8个电子 C.该原子中子数是86
D.1mol气体氡的质量大约是444g
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2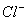 + 2H+
+ 2H+  H2↑+ Cl2↑
H2↑+ Cl2↑
B.用银氨溶液检验乙醛中的醛基:
CH3CHO +2Ag(NH3)2+ + 2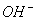

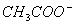 +
+ 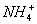 +3NH3 + 3Ag↓+ H2O
+3NH3 + 3Ag↓+ H2O
C.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2
2C6H5OH + 2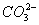
D.Na2SO3溶液使酸性KMnO4溶液褪色:5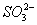 + 6H+ + 2MnO4- == 5
+ 6H+ + 2MnO4- == 5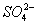 + 2Mn2+ 3H2O
+ 2Mn2+ 3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的二元酸H2A溶液的pH=4.0,则下列说法正确的是 ( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将衡氨水与稀盐酸混合时,不可能出现的结果是 ( )
A.pH>7,c(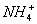 )+c(H+)=c(
)+c(H+)=c(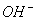 )+c(
)+c( )
)
B.pH<7,c(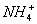 )+c(H+)=c(
)+c(H+)=c(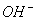 )+c(
)+c( )
)
C.pH=7,c(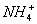 )> c(
)> c( )>c(H+)=c(
)>c(H+)=c(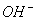 )
)
D.pH<7, c( )>c(
)>c(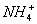 )> c(H+)>c(
)> c(H+)>c(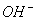 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.lmol· 醋酸溶液加水稀释,下列说法正确的是( )
醋酸溶液加水稀释,下列说法正确的是( )
A.溶液中c(H+)和c(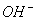 )都减小 B.溶液中c(H+)增大
)都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定的温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.C分解速率与B生成速率相等 B.A、B、C的浓度不再变化
C.单位时间生成n mol A,同时生成3n mol B
D.A、B、C的分子数之比为132
查看答案和解析>>
科目:高中化学 来源: 题型:
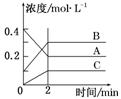
下图所示为800 ℃ 时A、B、C三种气体在密闭容器中反应时浓度的变化,只分析图形不能得出的结论是
A.A是反应物
B.前2 min A的分解速率为0.1 mol·L-1·min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.反应的方程式为:2A(g)  2B(g) +C(g)
2B(g) +C(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1;
FeO(s)+CO(g) △H1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
①反应CO2(g) + H2(g) CO(g) + H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g)
CO(g) + H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
②能判断CO2(g) + H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
 ⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)
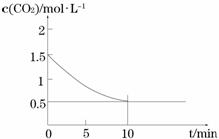
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。
① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为_________mol·L-1。
②下列措施中能使平衡时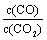 增大的是______(填序号)。
增大的是______(填序号)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com