
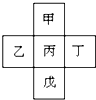
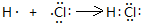 ,
,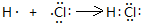 ;
;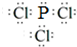 ,故答案为:
,故答案为: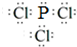 ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| X | Y | ||
| Z | W | M |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 3 |
| 4 |
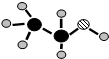
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.短周期元素形成离子后,最外层均达8电子稳定结构 |
| B.多电子原子中,在离核较近的区域运动的电子能量较低 |
| C.非金属元素组成的化合物中只有共价键 |
| D.HF、HCl、HBr、HI的热稳定性和还原性依次增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔融状态能导电的物质一定是离子化合物 |
| B.ⅠA族和ⅦA族元素原子化合时,一定形成离子键 |
| C.任何分子内一定存在化学键 |
| D.H2O分子的形成是H、O原子相互提供电子,使其最外电子层都达到稳定结构并产生强相互作用的结果 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com