
下列各组离子在溶液中能大量共存,加入OH﹣有沉淀生成,加入H+有气体生成的一组离子是( )
|
| A. | K+、Mg2+、Cl﹣、HCO3﹣ | B. | K+、Cu2+、SO42﹣、Na+ |
|
| C. | NH4+、CO32﹣、NO3﹣、Na+ | D. | NH4+、Cl﹣、HCO3﹣、K+ |
考点:
离子共存问题.
专题:
离子反应专题.
分析:
根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,再结合加入OH﹣有沉淀生成,加入H+有气体生成来解答.
解答:
解:A.该组离子之间不反应,可大量共存,加入OH﹣有氢氧化镁沉淀生成,加入H+有二氧化碳气体生成,故A选;
B.该组离子之间不反应,可大量共存,但加H+没有气体生成,故B不选;
C.该组离子之间不反应,可大量共存,但加OH﹣没有沉淀生成,故C不选;
D.该组离子之间不反应,可大量共存,但加OH﹣没有沉淀生成,故D不选;
故选A.
点评:
本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意与酸、碱的反应,题目难度不大.


科目:高中化学 来源: 题型:
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到氢气bmol,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为( )
A. 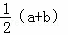 mol B. (a﹣b)mol C.
mol B. (a﹣b)mol C. 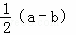 mol D. (a+b)mol
mol D. (a+b)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数,下列说法中正确的是( )
|
| A. | 7.8g过氧化钠固体中含阴离子个数为0.2NA |
|
| B. | 34g氨气中含N﹣H的数目为6NA |
|
| C. | 标准状况下,22.4L乙炔中含π键数为2NA |
|
| D. | 1molNaHSO4晶体中阳离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是(N0表示阿伏加德罗常数的值)( )
①在常温常压下,11.2L N2含有的分子数为0.5N0
②在常温常压下,1mol Ne含有的原子数为N0
③71g Cl2所含原子数为2N0
④在同温同压时,相同体积的任何气体单质所含的原子数相同.
|
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
)实验室制取H2的反应方程式为:Zn+H2SO4═ZnSO4+H2↑.
(1) 是氧化剂; 是还原剂; 元素被氧化; 元素被还原; 是氧化产物; 是还原产物.
(2)用双线桥表示出该反应电子转移的方向和数目 :Zn+H2SO4═ZnSO4+H2.
查看答案和解析>>
科目:高中化学 来源: 题型:
2012年4月22日是第43个“世界地球日”,其主题为“绿色梦想,低碳行动”.下列做法符合这一主题的是( )
①开发太阳能、风能和氢能等能源;
②大量开采地下水,以满足生产、生活的需求;
③在含硫的煤中加入适量生石灰;
④利用苯、甲苯等有机物代替水作溶剂;
⑤利用可降解的“玉米塑料”生产一次性饭盒.
|
| A. | ①③⑤ | B. | ①②③ | C. | ②④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学﹣﹣选修化学与技术】
下图是某工厂对海水资源进行综合利用的示意图.

请回答下列问题:
(1)请列举一种海水淡化的方法 .;
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是 ,NaOH在电解槽的 室生成,由饱和食盐水制取NaOH的化学方程式为 ↑ ;
(3)侯氏制碱法中首先向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入
(填化学式),理由是 .再由NaHCO3制得纯碱,化学方程式为 .
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取.已知有关物质的熔沸点数据如下:
| MgO | MgCl2 | |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
结合表中数据和实际生产情况说明,工业上生产镁采用电解MgCl2而不是电解MgO的理由 . .
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中物质的分类组合正确的是( )
| A | B | C | D | |
| 强电解质 | Al2(SO4)3 | BaSO4 | HF | KClO3 |
| 弱电解质 | H3PO4 | H2O | CaCO3 | Al(OH)3 |
| 非电解质 | CO2 | NH3•H2O | NH3 | HI |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com