
【题目】分实验室用氢氧化钠固体配制1.0 mol·L-1的NaOH溶液250mL,回答下列问题:
(1)实验仪器:托盘天平、药匙、烧杯、玻璃棒、(量筒)、 。
(2)实验步骤:①计算:②称量,③溶解,④移液,⑤洗涤,⑥ ⑦摇匀。称量所需氯化钠的质量为 g。
(3)下列操作使所配溶液的浓度偏大的有________;
A.托盘天平的托盘放上纸称量NaOH |
B.未洗涤溶解NaOH的烧杯 |
C.溶解后未冷却就立即转移到容量瓶中 |
D.定容时俯视刻度线 |
E.摇匀,静置后发现液面不到刻度线,再加水至刻度线
F.容量瓶未干燥即用来配制溶液
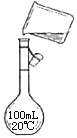
(4)右图是实验步骤④的示意图,图中的错误是
【答案】(1) 250mL容量瓶,胶头滴管 ;
(2) 定容; 10.0,(3)C、D
(4)未用玻璃棒引流;未使用250 mL容量瓶
【解析】试题分析:(1) 配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、移液、洗涤、定容,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,所以还缺少的仪器:250mL容量瓶,胶头滴管,故答案为:250mL容量瓶,胶头滴管;
(2) 配制1.0 mol·L-1的NaOH溶液250mL,依据配制步骤:计算、称量、溶解冷却、移液、洗涤、定容、摇匀装瓶,应该选用250mL容量瓶,所以必须配置250mL溶液,则需要m(NaOH)=cVM=1.0mol/L×0.25L×40g/mol=10.0g,故答案为:定容;10.0;
(3)A.托盘天平的托盘放上纸称量NaOH,氢氧化钠吸收空气中的水蒸气,导致溶质的物质的量偏小,浓度偏小,错误;B.未洗涤溶解NaOH的烧杯,导致溶质的物质的量偏小,浓度偏小,错误;C.溶解后未冷却就立即转移到容量瓶中,导致溶液的体积偏小,浓度偏大,正确;D.定容时俯视刻度线,导致溶液的体积偏小,浓度偏大,正确;E.摇匀,静置后发现液面不到刻度线,再加水至刻度线,导致溶液的体积偏大,浓度偏小,错误;F.容量瓶未干燥即用来配制溶液,对实验结果无影响,错误;故选CD;
(4)根据图示,图中的错误有未用玻璃棒引流;未使用250 mL容量瓶,故答案为:未用玻璃棒引流;未使用250 mL容量瓶。


科目:高中化学 来源: 题型:
【题目】把1mol X和1mol Y混合于2 L的密闭容器中,发生如下反应 2X(g)+Y(g) =nZ(g)
+2W(g),2min末X的物质的量为0.2mol,以Z的浓度表示的反应速率为0.1mol/(L·min)
请回答:
(1)前2min以X的浓度表示的平均反应速率
(2)n值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急。
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热ΔH= 。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成。
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:
CH3OCH3+6CO![]() -12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
-12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2。某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为 。
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气。
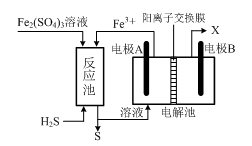
①电解池中电极A、B均为惰性电极,其中A为电解池的 极;电极B所得到的物质X的分子式为 。
②反应池中发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质,A是红色固体,B是黑色固体,各物质间的转化关系如下图,根据推断写出下列物质的化学式:A. ,B. ,C. ,D. 。
写出C生成D的化学方程式 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
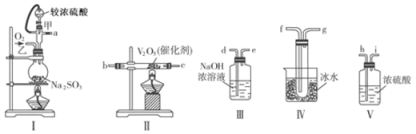
(1)写出I中用70%的硫酸和亚硫酸钠制取二氧化硫的化学方程式 。
(2)这些装置的连接顺序(按气体从左到右的方向)是a→ → → → → → → →d(填各接口的编号)。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。II中发生的化学方程式为 。
(4)Ⅳ处观察到的现象是 。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会 。(填“填大”“不变”或“减小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A. | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B. | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C. | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D. | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组收集了一种合金进行以下探究(已知铜元素的焰色反应呈绿色)。
(1)外观暗灰色,表皮光滑;
(2)在酒精灯外焰上灼烧,火焰呈绿色,合金片熔化,但不滴落;
(3)取刮去表皮的合金10 g,放入足量的稀硫酸中,收集到标准状况下的H2 8.96 L;
(4)另取刮去表皮的合金10 g,放入足量的NaOH溶液中,也收集到标准状况下的H2 8.96 L。
试据此判断,该合金中一定含有的元素是________(写元素符号);可能含有的元素是________(填选项编号)。
a.Ag b.Mg
c.Na d.Fe
如果该合金中只含2种元素,则二者的质量比是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com