
| 0.704-0.32 |
| 16 |


科目:高中化学 来源: 题型:
| A、铝与盐酸反应:Al+6H+=Al3++3H2↑ |
| B、稀盐酸与氢氧化铜反应:H++OH-=H2O |
| C、碳酸钠与氯化钙混合:CO32-+Ca2+=CaCO3↓ |
| D、澄清石灰水与盐酸反应:Ca(OH)2+2H+=2H2O+Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
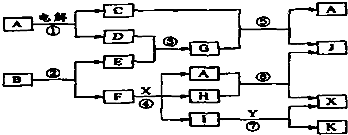
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A.化学常识 | B.化学与食品 |
| ?空气的主要成分--氮气和氧气 ?硬 水 和 软 水--可用肥皂水来检验 | ?甲 醛--浸泡肉类食品,以防变质 ?工业盐--用来腌制凉果、酸菜等食物 |
| C.化学与生活 | D.化学与能源 |
| ?人体缺铁--会引起贫血症 ?化纤织物、纯毛织物--用灼烧闻气味来鉴别 | ?沼气、酒精--生物能源,可再生能源 ?石 油、煤--化石能源,不可再生能源 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应的H2或溴水中Br2的最大量分别是( )
反应的H2或溴水中Br2的最大量分别是( )| A、11mol,9mol |
| B、9 mol,6mol |
| C、6mol,5 mol |
| D、l3 mol,9mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH2=CH-CH=CH2 |
| B、CH2=CH-CH3 |
| C、CH2=CH2 |
| D、以上答案均不合理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com