
��15�֣�����ʯ�к��е���Ҫ��������������������ij��ѧ��ȤС���ô���ʯΪԭ����ȡ��ȫ��ɱ�����������Ƶ���Ҫ���̣�
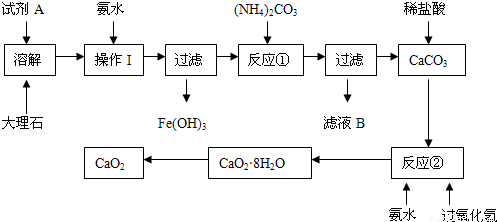
��ش��������⣺
��1���Լ�A�������� ��
��2������I��Ŀ���� ��
��3����ʵ����Ҫ���ʹ�ò���������ʵ������в������������� ��
��4��д����Ӧ��������CaO2��8H2O�Ļ�ѧ����ʽ�� ��
��5���Ƶõ�CaO2��һ�㺬��CaO�û�ѧ��ȤС��ͨ��ʵ��ⶨ�Ƶõ���Ʒ��CaO2�ĺ���������0.6g��Ʒ����ƿ�У�Ȼ����������Ũ��Ϊ2.00mol?L-1������20.00mL������Ũ��Ϊ2.00mol?L-1������������Һ�ζ���ƿ�е���Һ����������������Һ11.00mL������Ʒ��CaO2����������Ϊ ��
��1���������� ��2��������Һ��pH��ʹFe3+��ȫ��������3�������������
��4��CaC12 + H2O2 + 2NH3 + 8H2O �T CaO2��8H2O�� + 2NH4Cl ����5��72%��
��������
���������CaCO3����ϡHCl��ϡ���ᷢ����Ӧ��ת��Ϊ���������ʣ���������CaCO3��Ӧ���������������ˮ��ʹ��Ӧ���ܼ������С���Fe2O3�����ᷴӦ�õ������Ե����Σ�����Լ�A������������2�������м��백ˮ��Ŀ���ǵ�����Һ��pH��ʹFe3+��ȫ������Ȼ����˳�ȥ����3����ʵ����Ҫ���ʹ�ò���������ʵ������в������������дٽ������ܽ�Ľ����Ϊ�˷��������Թ������������Һ�ķ���������������ã���4����Ӧ������CaCO3��H2O2 �Ͱ�ˮ��Ӧ����CaO2��8H2O�Ļ�ѧ����ʽ�ǣ�CaC12 + H2O2 + 2NH3 + 8H2O �T CaO2��8H2O�� + 2NH4Cl ����5��n(HCl)= 2.00mol/L��0.02L=0.04mol��n(NaOH)=n(HCl)(����)= 2.00mol/L��0.011L-0.022mol�������Ʒ������OH-�����ʵ���Ϊ0.018mol.������Ʒ�к���CaO2��CaO�����ʵ����ֱ�x��y����2x+2y=0.018mol��72x+56y=0.6g�����x=0.006mol��y=0.003mol�����Ը���Ʒ��CaO2����������Ϊ[(0.006mol��72g/mol)��0.6]��100%=72%��
���㣺�����Լ���ѡ��������ʹ�á�ʵ�������Ŀ�ġ����ӷ���ʽ����д�����ʴ��ȵļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ��и�һ��ѧ����ĩѧ����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��д��ȷ����
A����Ba(OH)2��Һ�е���ϡ���H+ + OH��= H2O
B����AlCl3��Һ�е��백ˮ��Al3����3OH��= Al(OH)3��
C����NaHCO3��Һ�е���ϡ���H����HCO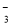 = CO2����H2O
= CO2����H2O
D����Fe2(SO4)3��Һ�м������ۣ�Fe3+��Fe = 2Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ����껨����һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
пƬ��̼���õ������Ӻ����ϡ�����У�пƬ��
A������ B������ C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������Ǩ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��W��R��5�ֶ�����Ԫ��,��ԭ��������������X�����ڱ���ԭ�Ӱ뾶��С��Ԫ��,Yԭ�������������Ǵ�����������3����Z��W��R����ͬһ���ڣ�R��Y����ͬһ�壬Z��Wԭ�ӵĺ��������֮����Y��Rԭ�ӵĺ��������֮����ȡ�����˵����ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������Ǩ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����¶�����ȫ�ѻ������������壬�������������ˮ������ʣ�������ƽ����������Ϊ21.6����ԭ���ֻ�������ƽ������������
A��21.6 B��27.6 C��29 D��36.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������б�ҵ��5�¸߿����ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ǧ�������ִ��������й㷺Ӧ�ã���缫������Pb ��PbO2�����Һ��H2SO4��Һ������Ǧ���ص�ⱥ����������Һһ��ʱ�䣬������ʱ�¶Ȳ������ö��Ե缫������˵������ȷ����
A�����طŵ�ʱ����·��ÿת��2 mol���ӣ������1 molPbO2����ԭ
B�����ص�������ӦʽΪ��4OH--4e-=2H2O+O2��
C������ c(Na2SO4)���䣬����Һ���о�������
D��������ÿ����1mol H2O�������о�����1mol H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������ѧ�ڸ߶��꼶��ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣�ijС��ͬѧ����H2C2O4��Һ������KMnO4��Һ��Ӧ��̽���������Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��������Թ���Ѹ����Ͼ��ȣ��ټ������ᣬ��ʼ��ʱ��ͨ���ⶨ�����Һ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������֪��Ӧ����ʽΪ��5H2C2O4+2KMnO4+3H2SO4��2MnSO4+K2SO4+10CO2��+8H2O������С����������·�����
��� | H2C2O4��Һ | KMnO4��Һ | ������Һ | �¶�/�� | ||
| Ũ�� ��mol/L�� | ��� ��mL�� | Ũ�� ��mol/L�� | ��� ��mL�� |
|
|
�� | 0��10 | 2��0 | 0��010 | 4��0 | 4mL 4mol/L | 25 |
�� | 0��20 | 2��0 | 0��010 | 4��0 | 4mL 4mol/L | 25 |
�� | 0��20 | 2��0 | 0��010 | 4��0 | 4mL 4mol/L | 50 |
��1��̽���¶ȶԻ�ѧ��Ӧ����Ӱ������ʵ������__________�����ţ���ͬ����̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ������ʵ������__________��
��2����С��ͬѧ�ɴ�ʵ�鷢�ַ�Ӧ����һЩʱ�����һʱ��η�Ӧ���ʲ��ϼӿ졣ͬѧ�Ƿ������˷�Ӧ����ʹ��ϵ�¶������⣬���ܻ�������ԭ���������뵽�̲��ϵĿ�ѧ̽��ʵ�飬�ƶϳ���Ӧ�����Һ�е�__________���ѧʽ��Ҳ�����˴˷�Ӧ�Ľ��С�
��3������ʵ����г�ַ�Ӧ��H2C2O4������������������ͨ��������KMnO4��Һ�ζ��ķ������ⶨ��Ӧ���Һ�й�����H2C2O4����ش��������⣺
��ȡ�÷�Ӧ���Һ�ĵζ�����__________�ζ��ܣ����ʽ����ʽ������ͬ����ʢװKMnO4��Һ�ĵζ�����__________�ζ��ܡ�
�����в����п���ʹ�����H2C2O4ʣ����������ֵƫ�͵���__________��
A�� ��ȡ����KMnO4��Һ���ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
B�� �ζ�ǰʢ�ŷ�Ӧ���Һ����ƿ������ˮϴ����û�и���
C�� ʢװKMnO4��Һ�ĵζ��ܵζ�ǰ�����ݣ��ζ���������ʧ
D�� ʢװKMnO4��Һ�ĵζ���δ��ϴ��ֱ��ע������KMnO4��Һ
�۴˵ζ�ʵ���Ƿ���Ҫ�μ�ָʾ��________����ǡ�������ôȷ���˵ζ����յ㣺_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������ѧ�ڸ߶��꼶��ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ƽ�ⳣ���У���ʾ������Ӧ�̶�������
A��K�� B��K��
B��K�� C��K��1 D��K��1010
C��K��1 D��K��1010
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���л�ѧ������ȷ����
A��H2O2�ĵ���ʽ�� | B��������ӵ����ģ�ͣ� |
C��CO2�ı���ģ�ͣ� | D��ԭ�Ӻ�����20�����ӵ���ԭ�ӣ�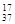 Cl Cl |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com